氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产.生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) =" 2" N2(g)+CO2(g) + 2H2O(g) ΔH2、
若1 mol CH4 还原NO2 至N2,整个过程中放出的热量为867 kJ,则ΔH2= ;
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2 2NH3,则在电化学合成氨的过程中,阴极反应式为 ;
2NH3,则在电化学合成氨的过程中,阴极反应式为 ;
(3)在一定条件下,将l mol N2 与3 mol H2 混合于一个10 L密闭容器中,反应达到平衡时,A点混合气体中氨占25%,试回答:
①A点时N2的浓度为 mol/L;
②右图中在状态A时,平衡常数 KA = (填写代入数值的表达式,不要求化简);当温度由T1变化到T2时,KA KB(填“>”、“<”或“=”)。
③在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 时间/min 浓度/mol•L—1 |
c (N2) |
c (H2) |
c (NH3) |
| 0 |
0.6 |
1.8 |
0 |
| 3 |
0.52 |
x |
0.16 |
| 6 |
0.36 |
1.08 |
0.48 |
| 9 |
0.36 |
1.08 |
0.48 |
反应从0 min到3 min之间,H2的反应速率为 ;反应在3 min时,条件发生了改变,改变的条件可能是 (填序号)。
a.使用催化剂 b.降低温度 c.增加H2的浓度 d.充入Ne增大压强
(1)某肉制品包装上印有相关配料:精选瘦肉、食盐、胭脂红、苯甲酸钠。其中属于调味剂的是,属于着色剂的是,属于防腐剂的是。
(2)亚硝酸钠有毒,其外观和咸味与食盐很相似,因此要防止因误食亚硝酸钠而发生事故。亚硝酸钠和氯化钠的部分性质如下表:
| 性质 |
亚硝酸钠 |
氯化钠 |
| 1.酸性条件下的稳定性 |
微热时分解为NO和NO2 |
微热时不分解 |
| 2.熔点 |
271℃ |
801℃ |
| 3.室温时的溶解度 |
约80g |
约35g |
①请根据表中信息设计一种鉴别NaNO2和NaCl的方法,写出简单的操作过程、现象和结论:
②碘是人体中不可缺少的(选填“常量”或“微量”)元素。
③食盐中加入碘元素能有效防止缺碘引起的疾病。以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%。现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%。食盐中加入碘化钾的碘损失率高的原因是;(填字母)。
a.碘化钾被氧化,造成碘化钾的碘损失率高。
b.碘化钾升华,造成碘化钾的碘损失率高。
c.碘化钾与食物中的成分发生反应,造成碘化钾的碘损失率高。
④萃取碘水中的碘时,一般选用的试剂是(填字母);
A.酒精 B.四氯化碳C.乙酸
⑤可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾。反应化学方程式为:
5KI+KIO3 + 6HCl ="=" 6KCl + 3I2 + 3H 2O,反应的现象是
2O,反应的现象是
⑥已知碘酸钾受热易分解,你认为在用碘酸钾加碘盐进行烹饪时应注意什么问题?。
⑶糖类、油脂、蛋白质都是人体必需的营养物质。
①油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和(写结构简式)。人体中共有二十多种氨基酸,其中人体自身_____(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
③淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:。
溶液中可能含有H+、K+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,
⑴、该溶液中肯定含有的离子是,且各离子的物质的量之比为;肯定不含的离子是。
⑵、还有一种离子可能存在,写出检验这种离子的实验方法及现象:
。
(1)油脂被摄入人体后,在酶的作用下水解为和甘油(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)发育出现障碍,患营养缺乏症,这主要是由于摄取_________(填“蛋白质”、“脂肪”或“糖类”)不足引起的。下列食物中富含该物质的是(填字母)。
| A.菠菜 | B.花生油 | C.瘦肉 | D.西瓜 |
(3)某品牌抗酸药的成分主要有糖衣、碳酸钙、淀粉等。
①写出该抗酸药发挥功效时的离子方程式:。
②淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,写出其水解方程式:。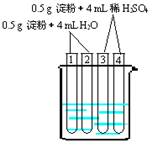
(4)上图所示4支试管同时水浴加热4min,为检验其中淀粉的水解程度,某同学的实验操作与现象记录如下:
| 编号 |
操作 |
现象 |
| 1 |
加入碘水 |
溶液变成蓝色 |
| 2 |
加入银氨溶液,水浴加热 |
未出现银镜 |
| 3 |
加入碘水 |
溶液变成蓝色 |
| 4 |
加入银氨溶液,水浴加热 |
未出现银镜 |
①结合试管1、2中的现象,得出的结论是,这两支试管中淀粉水解(填“没有”、“部分”或“全部”)。
②结合试管3、4中的现象,不能得出“这两支试管中淀粉没有水解”的结论,理由是
。
防治环境污染,改善生态环境己成为全球的共识。
(1)垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有(填字母)标志的垃圾筒内。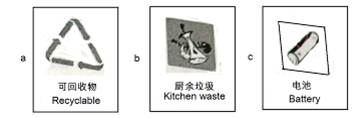
(2)工业废水需处理达标后才能排放。下列废水处理的方法合理的是(填字母)。
a.用中和法除去废水中的酸
b.用混凝法除去废水中的重金属离子
c.用氯气除去废水中的悬浮物
d.用氧化还原法除油类、氰化物
(3)为了减少煤燃烧产生的SO2对大气造成的污染,可向煤中加入适量石灰石。石灰石与煤燃烧时产生的SO2及空气中的O2反应,生成CaSO4和CO2,写出该反应的化学方程式:。
某芳香烃A有如下转化关系: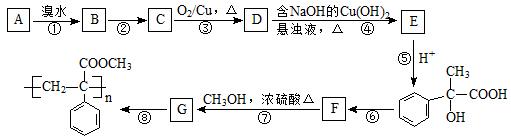
按要求填空:
⑴写出反应②和⑥的反应条件:②;⑥。
⑵写出A和G结构简式:A;G。
⑶写出反应③对应的化学方程式:;
⑷写出反应⑦对应的化学方程式:。
⑸属于取代反应的有(填序号),反应⑧的反应类型属于。