(13分) 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素。D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B。
请回答:
(1)A元素的名称是________________;
(2)B元素的轨道表示式是________________,C的原子结构示意图是________________,B与A形成的化合物比C与A形成的化合物沸点高,其原因是__________________________________________________________;
(3)E属于元素周期表中第________周期,第________族的元素,其元素名称是________;属于元素周期表中的 区(填元素分区),它的+2价离子的电子排布式为________________;
(4)从图中可以看出,D跟B形成的离子化合物的化学式为________________;该离子化合物晶体的密度为a g?cm-3,则晶胞的体积是________________(只要求列出算式)。
(8分)以 ①2NaOH+ Cl2 NaCl+NaClO+H2O② 2Na + Cl2
NaCl+NaClO+H2O② 2Na + Cl2 2NaCl
2NaCl
③ 2Fe3+ + 2I– 2Fe2+ + I2 ④ 2Fe2+ + Br2
2Fe2+ + I2 ④ 2Fe2+ + Br2 2Fe3+ + 2Br–
2Fe3+ + 2Br–
这四个反应为例,我们来探究氧化还原反应。
(1)氧化还原反应的本质是。
(2)对于反应①,氧化剂是。
(3)对于反应②,Na的化合价由0价变成+1价,化合价升高的原因是。
(4)由③、④两反应,可以推断Fe3+、Br2、I2的氧化性强弱顺序为。
(1)鉴别KCl溶液和K2CO3的试剂是 ,离子方程式为 。
(2)除去混入NaCl溶液中少量NaHCO3杂质的试剂是 ,离子方程式为 。
(3)除去Na2CO3粉末中混入的NaHCO3杂质用 方法,化学方程式为 。(3分)
A、B是中学化学里常见的物质,其中B是单质,A是化合物。各物质之间的转化关系如图所示: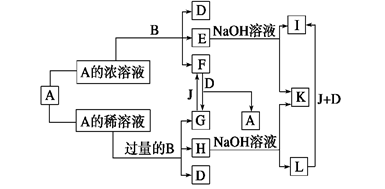
已知:往E溶液中滴加KSCN溶液时,溶液呈红色; A的浓溶液与B在常温下无明显反应现象。请回答:
(1)框图中B和A的浓溶液反应的条件是,而常温下无明显现象的原因是 _________ ____________________________________________ ;
(2)写出F和G相互转化的化学方程式:
F→G:;
G→F: __________ ;
(3)L转化成I的化学方程式是_____________________________________________。
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示:
由此可知,(1)该溶液中肯定含有的阳离子是____________________,且各阳离子的物质的量之比为_____________;肯定不含有的阳离子是___________;检验可能含有的某种阳离子的常用实验方法是;
(2)分别写出BC、CD段对应的离子方程式,并写出BC段参加反应的阳离子在实验室中常用的检验其存在的方法:BC:________________________________________;
检验:_____________________________________________;
CD:__________________________________________.
用质量分数为98%、密度为1.84g·cm-3的浓硫酸配制100mL 1.84mol·L-1的稀硫酸,若实验仪器有:
| A.100mL量筒; | B.托盘天平; | C.玻璃棒; | D.50mL容量瓶; |
E.10mL量筒,F.胶头滴管;G.50mL烧杯;H.100mL容量瓶
实验时应选用仪器的先后顺序是(填入编号):_______________________________。