(8分)以 ①2NaOH+ Cl2 NaCl+NaClO+H2O ② 2Na + Cl2
NaCl+NaClO+H2O ② 2Na + Cl2 2NaCl
2NaCl
③ 2Fe3+ + 2I– 2Fe2+ + I2 ④ 2Fe2+ + Br2
2Fe2+ + I2 ④ 2Fe2+ + Br2 2Fe3+ + 2Br–
2Fe3+ + 2Br–
这四个反应为例,我们来探究氧化还原反应。
(1)氧化还原反应的本质是 。
(2)对于反应①,氧化剂是 。
(3)对于反应②,Na的化合价由0价变成+1价,化合价升高的原因是 。
(4)由③、④两反应,可以推断Fe3+、Br2、I2的氧化性强弱顺序为 。
在碱性废水的处理中,通常用于烟道气处理。在充分燃烧的烟道中,大约含有14%的CO2,将烟道气通入碱性废水中进行中和处理,是比较先进而经济的办法,写出该处理方法的离子方程式。
把下列离子方程式改写成化学方程式
(1)CO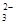 +2H+
+2H+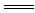 CO2↑+H2O
CO2↑+H2O
(2)Ag++Cl-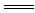 AgCl↓
AgCl↓
(3)Cu2++2OH-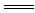 Cu(OH)2↓
Cu(OH)2↓
(4)Ba2+十SO42-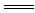 BaSO4
BaSO4 ↓
↓
物质的量相等的 CO 和 CO2中,分子个数之比为;原子个数之比为;氧原子个数比为。
现有A、B、C、D、E五种核电荷数小于18的元素,其中:A原子核内无中子,B原子最外层电 子数是次外层的2倍,C原子最外层电子数是其电子层数的3倍,D原子核外K层比M层电子数多1,,E形成的-1价离
子数是次外层的2倍,C原子最外层电子数是其电子层数的3倍,D原子核外K层比M层电子数多1,,E形成的-1价离 子与Ar原子核外电子排布相同;
子与Ar原子核外电子排布相同;
由此推知:
(1)A原子符号是;
(2)B原子结构示意图是
(3)E元素形成的单质与A、C、D三元素形成呈碱性的化合物反应的方程式:
现有以下物质:
①干燥的食盐晶体②镁③熔化的KNO3④蔗糖⑤MgCl2溶液
⑥液态硫酸⑦酒精⑧氯水⑨石墨⑩SO3,
请回答:
(1)以上物质中能导电的是;(填序号)
(2)以上物质中属于非电解质的是;(填序号)