某学生查阅资料得知溴乙烷的物理性质与制取方法如下表:
联想到所学溴苯的制取,他设了制取溴苯和溴乙烷的装置I,主要实验步骤如下:
①检查气密性后,向烧瓶中加入一定量的苯和液溴。
②向锥形瓶中加入乙醇和浓硫酸的混合液至恰好于进气导管口。
③将A装置中的纯铁丝向下插入混合液中。
④点燃B装置中酒精灯,用小火缓缓对锥形瓶加热10min.请填写下列空白: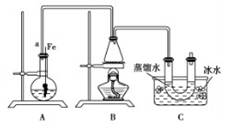
(1)A中发生反应的方程式
(2)装置长导管a的作用是
(3)C装置中的U形管内用蒸馏水封住管底的作用是
(4)反应完毕后,U形管内的现象是 分离出溴乙烷时所用的最主要的仪器名称是 (只填一种)
可以从以下角度判断氯元素和硫元素非金属性的强弱:
(1)在元素周期表中,氯元素和硫元素的相对位置是__________________________,根据____________________________规律来判断氯元素和硫元素非金属性的强弱。
(2)二者气态氢化物中______________(填化学式)更易分解,由此可判断氯元素和硫元素非金属性的强弱。
(3)向硫化氢溶液中通入氯气,溶液变浑浊,反应的化学方程式为__________________,说明氯元素的非金属性比硫元素________________(填“强”或“弱”)。
(4)氯气和硫分别与铁形成化合物的化学式为________________和________________,据此也可判断氯元素和硫元素非金属性的强弱。
根据下表,用化学式或元素符号完成下列问题:
| O |
F |
| S |
Cl |
| Se |
Br |
| Te |
I |
(1)非金属性最强的元素是_________________。
(2)还原性最强的离子是________________。
(3)H2Te的稳定性比HI(填“强”或“弱”)______________。
(4)已知:2F2+2H2O====4HF+O2,Cl2+H2S====2HCl+S↓,请完成下列化学方程式:
Br2+H2Se====________________。I2+H2Te====______________。
针对以下A—D四个涉及H2O2的反应(未配平):
A.Na2O2+HCl H2O2+NaCl H2O2+NaCl |
B.Ag2O+H2O2 Ag+O2+H2O Ag+O2+H2O |
C.H2O2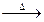 H2O+O2 H2O+O2 |
D.H2O2+Cr2(SO4)3+KOH K2SO4+K2CrO4+H2O K2SO4+K2CrO4+H2O |
请完成下列问题:
(1)H2O2仅表现氧化性的反应是_______________(填编号,下同),并配平此化学反应方程式:______________________。
(2)H2O2既表现氧化性又表现还原性的反应是___________。
(3)H2O2仅表现弱酸性的反应是___________,其理由为__________________________。
(10分)含有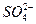 、
、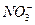 、
、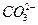 、CH3COO-离子的溶液中加入足量的硫酸,明显减少的阴离子有_________,明显增加的阴离子有_________,再加入足量BaCl2溶液,阴离子明显减少的是_________,增加的阴离子有_________,再加入足量AgNO3溶液,最后溶液中留下的的阴离子为_________。
、CH3COO-离子的溶液中加入足量的硫酸,明显减少的阴离子有_________,明显增加的阴离子有_________,再加入足量BaCl2溶液,阴离子明显减少的是_________,增加的阴离子有_________,再加入足量AgNO3溶液,最后溶液中留下的的阴离子为_________。
(8分)写出下列反应的离子方程式
(1)澄清石灰水中通入少量二氧化碳
____________________________________________________________________________
(2)石灰石溶于醋酸中
____________________________________________________________________________
(3)铁和硫酸铜溶液
____________________________________________________________________________
(4)碳酸氢钠溶液与氢氧化钠溶液
____________________________________________________________________________