1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为
| A.C + H2O ==CO + H2 ; ΔH==+131.3KJ·mol—1 |
| B.C(s)+ H2O(g) ==CO(g) + H2(g) ; ΔH==+10.94KJ·mol—1 |
| C.C(s)+ H2O(l) ==CO(g) + H2(g) ; ΔH==+131.3KJ·mol—1 |
| D.C(s)+ H2O(g) ==CO(g) + H2(g) ; ΔH==+131.3KJ·mol—1 |
同温同压下,等体积的两容器内分别充满14N16O和13C16O气体,下列对两容器中气体判断正确的是
| A.中子数相同 | B.分子数不同 | C.质子数相同 | D.气体质量相同 |
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是
| A.2.24 L CO2中含有的原子数为0.3×6.02×1023 |
| B.0.1 L 3 mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 |
| C.5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 |
| D.4.5 g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
下列离子方程式中,正确的是高
A.水玻璃中通入足量的CO2: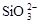 +2CO2+2H2O==H2SiO3 (胶体)+2CO +2CO2+2H2O==H2SiO3 (胶体)+2CO |
| B.氯化亚铁溶液中通入足量的Cl2:2Fe2++Cl2==2Fe3++2Cl- |
C.NaHCO3溶液中加入足量NaHSO4溶液: 2H++CO ==CO2↑+H2O ==CO2↑+H2O |
| D.碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
11P + 15CuSO4 + 24H2O = 5Cu3P + 6H3PO4 + 15H2SO4 反应中,被氧化的P原子与被还原的P原子个数比是
| A.6:5 | B.5:6 | C.11:5 | D.11:6 |
20℃时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1,则下列说法中正确的是
| A.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174 g·cm-3 |
B.此溶液中KCl的质量分数为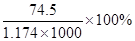 |
| C.密度大于1.174 g·cm-3的KCl溶液是过饱和溶液 |
| D.25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1科网 |