常温下,取0.2 mol/L HA溶液与0.2 mol/L NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
(1)混合后的溶液中由水电离出的c(OH-)____0.1 mol/L NaOH溶液中由水电离出的c(OH-)(填“>”、“<”或“=”)。
(2)已知NH4A溶液显中性,又知将HA溶液加到NaHCO3溶液中有气体放出,试推断NH4HCO3溶液的pH________7(填“>”、“<”或“=”)。
(3)有相同温度下相同浓度的四种盐溶液:
| A.NH4HCO3; | B.NH4A; | C.(NH4)2SO4; | D.NH4Cl |
按pH由大到小的顺序排列__________________(填字母序号)。
烯烃中碳碳双键是重要的官能团,在不同条件下能发生多种变化。
(1)烯烃的复分解反应就是两种烯烃交换双键两端的基团,生成两种新烯烃的反应。请写出在催化剂作用下,两个丙烯分子间发生复分解反应的化学方程式____________________________。
(2)烯烃与高锰酸钾酸性溶液反应的氧化产物有如下的反应关系: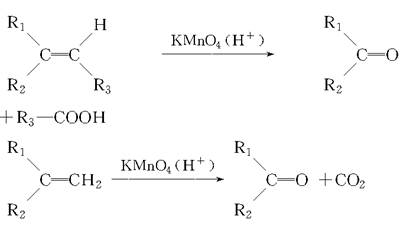
已知某烯烃的化学式为C5H10,它与高锰酸钾酸性溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是________________;若为二氧化碳和丁酮(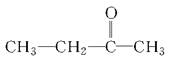 ),则此烯烃的结构简式是________。
),则此烯烃的结构简式是________。
最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下: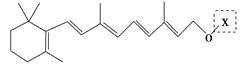
为了研究X的结构,将化合物A在一定条件下水解只得到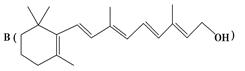
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应B.加成反应
C.缩聚反应D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。
(ⅰ)写出有机物的结构简式:D:______________,
C:________________,E:__________________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;
反应⑥__________________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
根据下述转化关系,回答问题: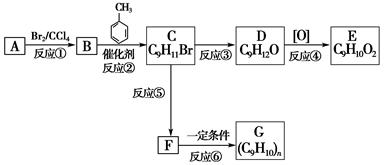
已知:①+CH3Br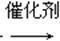 CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
由碳、氢、氧3种元素组成的有机物A,相对分子质量为152,其分子中C、H原子个数比为1∶1,氧元素的质量分数为31.58%。A遇FeCl3溶液显紫色,A能与NaHCO3溶液反应,其苯环上的一氯取代物有两种,请回答下列问题:
(1)A的分子式是____________________________________;
(2)A的结构简式为___________________________________;
(3)A可以发生如图 所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式__________________________________。
所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式__________________________________。
(4)甲、乙两装置均可用作实验室由C制取B的装置,乙图采用甘油浴加热(甘油沸点290 ℃,熔点18.17℃),当甘油温度达到反应温度时,将盛有C和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度。甲、乙两装置相比较,乙装置有哪些优点________。
葡萄糖是人类的营养素。在人体里,富氧条件下氧化生成二氧化碳和水;在缺氧时则生成一种有机酸A。已知:

回答下列问题:
(1)C和D′属于________(填编号,以下同)。
①同系物 ②同分异构体
③同类物质 ④同素异形体
(2)D′和E分别属于哪一类化合物:D′________,E________。
①多元醇 ②醛 ③不饱和羧酸 ④多元羧酸 ⑤酯
(3)写出结构简式:A ____________,F ________________,
H________。
(4)写出反应类型:Ⅰ________,Ⅱ________。
(5)写出A→E的化学方程式:_______________________。