(1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在可以设计成原电池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应的电极反应式为 。
(3)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与下图中
电解池相连,其中,a为电解液,X和Y是两块电极板,则: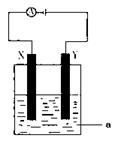
① 若X和Y均为惰性电极,a为CuSO4溶液,
则阳极的电极反应式为 ,电解时的化学反应方程式为 ,通过一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为
③若用此装置电解精炼铜, 做阳极,电解液CuSO4的浓度 (填“增大”、“减小”或“不变”)。
④若用此装置在铁制品上镀铜,铁制品做 ,电镀液的浓度 (填“增大”、“减小”或“不变”)。
在室温下,下列五种溶液:
① 0.1 mol/L CH3COONa②0.1 mol/L CH3COONH4
③0.1 mol/L NH4HSO4
④0.1 mol/L NH3·H2O和0.1 mol/L NH4Cl等体积混合
⑤0.1 mol/L NH3·H2O⑥0.1 mol/L NH4Cl
请根据要求填写下列空白:
(1)溶液①呈(填“酸性”、“碱性”或“中性”),其原因是(用离子方程式表示)。
(2)比较溶液②和③,其中c(NH4+)的大小关系是②______③(填“>”、“<”或“=”)。
(3)在混合液④中,c(Cl-)="________" mol/L;c(NH3·H2O)+ c(NH4+)______ 0.2 mol/L(填“>”、“<”或“=”)。
(4)室温下,一定体积的溶液⑤和溶液⑥混合后所得溶液的pH=7,则溶液中离子浓度的大小关系是:。
已知某溶液中只存在OH-、H+、NH4+、Cl-,某同学推测其离子浓度大小顺序可能有如下四种关系①c(Cl-)>c(NH4+)>c(H+)>c(OH-)②c(NH4+)>c(OH-)>c(Cl-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解一种溶质,则该溶质是,若四种离子的关系符合③,则溶质为若四种离子的关系符合④,则溶质为。
(2)将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数,则下面图象正确的是(填图象符号)________。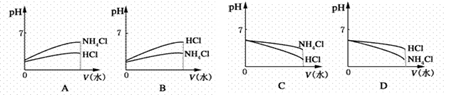
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”“小于”或“等于”)。
(4)在浓度均为0.1mol/L①CH3COONH4②NH4HSO4③NH4Cl ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为(填序号)
(5)已知:0.5 mol液态肼(N2H4)与足量的液态双氧水反应,生成氮气和水蒸气,放出256.65 kJ的热量.反应的热化学方程式为:。
已知A(g)+B(g) 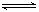 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ |
700 |
900 |
830 |
1000 |
1200 |
| 平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
回答下列问题:
(1)该反应的 △H0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,若反应经一段时间后,达到平衡时A的转化率为,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率会(填“变大”、“变小”或“不变”)
(3)若保持容器的容积不变,则该反应达到化学平衡状态的依据是________(填序号)。
a.单位时间里生成B和D的物质的量相等
b.气体的密度不随时间改变
c.容器内压强保持不变
d.混合气体的平均摩尔质量保持不变
(4)1200 ℃时反应C(g)+D(g) 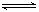 A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。
(1)请写出下列溶液的离子反应方程式:(13分)
①硫酸氢钠在溶液中的电离:
②氯化铵溶液除铁锈的原因:
③氯化铁溶液与偏铝酸钾溶液混合:
④碳酸钙的溶解平衡:
(2)在配制AgNO3溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,
以(填“促进”、“抑制”)其水解。在配制硫化钠溶液时,为了防止发生水解,可以加入少量的。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产是。把Na2SO3溶液蒸干,灼烧,最后得到的主要固体产是。
海藻中富含碘元素。某小组同学在实验室里用灼烧海藻的灰分提取碘,流程如下图。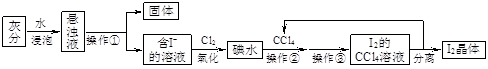
(1)写出操作名称:操作①,操作③。
(2)用NaOH浓溶液反萃取后再加稀酸,可以分离I2和CCl4。有关化学方程式为:
碱性条件,3I2+6NaOH=5NaI+NaIO3+3H2O,
酸性条件,5NaI+NaIO3+3H2SO4=3Na2SO4+3I2+H2O。
以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的(填仪器名称)中加入少量1mol·L-1 NaOH溶液;
②振荡至溶液的色消失,静置、分层,则(填“上”、“下”)层为CCl4;
③将含碘的碱溶液从仪器的(填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴1 mol·L-1 H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体;
(3)本实验中可以循环利用的物质是。