某同学在自主学习酸的知识时,设计了以下实验报告,请将实验报告补充完整。
【实验目的】
【实验用品】试管、铁片、铜片、稀盐酸、稀硫酸、NaOH溶液、石蕊和酚酞试液等
【实验内容】
| 实验 步骤 |
① |
②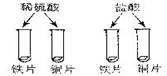 |
③ |
| 实验 现象 |
溶液变为 色 |
稀酸中的铁片表面都有 产生; 铜片表面都没有明显现象 |
溶液由红色变为无色 |
| 分析 与 结论 |
结论: 稀酸能与指示剂作用 |
铁与稀硫酸反应的化学方程式为 结论:稀酸能与较活泼金属反应 |
结论: 酸能 |
【实验思考】从物质组成的角度解释稀酸具有酸的通性的原因 。
根据下列制取氧气的装置图回答问题。
(1) 写出仪器①、②的名称①________________;②__________________。
(2) 实验室常用高锰酸钾或过氧化氢和二氧化锰来制取氧气,你认为其中相对较好的方法是______________________,其理由是。
(3)检验集气瓶中是否收集满氧气的方法是,将带火星的小木条放在,若木条,说明已满。
(4)何洁同学在制取氧气过程中,她收集一瓶氧气后,用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃。其原因可能是______________________________。
(5)若用排水法收集氧气,则导管口开始有气泡放出时,不宜立即收集,因为。实验即将结束时,应先,后。
某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究。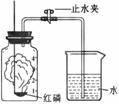
(1)如右图所示装置和药品进行实验,实验中可观察到的现象是: 。
(2)小明同学认为可用木炭代替红磷测定空气中氧气的含量,小丽同学认为不可以,其原因是: 。
(3)小芳同学用镁条代替红磷来测定空气中氧气的含量。结果却发现倒吸的水量远远超过集气瓶的1/5。小组内同学帮她仔细检查,发现装置的气密性及操作步骤均无问题。你认为造成此现象的原因可能是
(4)小组内同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是:
(5)小组内同学还对该实验进行了如下改进。(已知试管容积为 45 mL).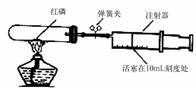
实验的操作步骤如下:①点燃酒精灯。②撤去酒精灯,待试管冷却后松开弹簧夹。③将少量红磷平装入试管中,将20 mL的注射器活塞置于10 mL刻度处,并按上图中所示的连接方式固定好,再将弹簧夹紧橡皮管。④读取注射器活塞的数据。
你认为正确的实验操作顺序是 (填序号)。注射器活塞将从10 mL刻度处慢慢前移到约为 mL刻度处才停止。
化学实验老师整理药品时,拿出一瓶久置的氢氧化钙粉末,他让小刘和小赵对这瓶氢氧化钙粉末的组成进行实验探究。
(1)提出问题:这瓶氢氧化钙是否已经生成碳酸钙而变质?
(2)进行猜想:药品可能有以下三种情况。
A.氢氧化钙全部变为碳酸钙;B.氢氧化钙部分变为碳酸钙;C.。
(3)设计实验方案、进行实验:下表是对猜想A进行实验探究的过程示例:
| 实验步骤 |
实验现象 |
实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 |
①滤液不变色 ②有气泡产生 |
氢氧化钙全部变为碳酸钙 |
请你另选择一种猜想参与探究,完成下表。
| 实验步骤 |
实验现象 |
实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 |
① |
|
| ② |
(4)原理与用途:
①农业上一般采用氢氧化钙改良性土壤(选填“酸”或“碱”)。
②氢氧化钙变质是由于与空气中的发生反应的缘故,因此氢氧化钙应保存。
实验是实现科学探究的重要途径。请回答以下有关问题: 
(1)仪器②的名称是_____________。
(2)用上图仪器组装成气体发生装置,该装置既可制取氢气又可制取氧气,应选(填序号)。写出实验室制取氧气的化学方程式。
(3)实验室制取二氧化碳,E装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是,若不加油层会使测定结果(填“偏大”或“偏小”)。
化学是一门实验科学,关注物质变化过程,探究物质变化的条件很有必要。某化学兴趣小组做了如下图所示的实验。
A.探究燃烧的条件 B.探究铁钉生锈的条件
根据上述实验,回答下列问题:
(1)实验A 是通过控制哪些因素来探究可燃物燃烧的条件?
(2)写出白磷燃烧的化学方程式
(3)实验B中,中间试管的实验目的是什么?
(4)请总结出铁制品发生锈蚀的主要条件
(5)写出防止铁制品锈蚀的一种方法。