从H、C、O、N、K、Ca六种元素中,选出适当的元素写出符合下列要求的物质的化学式。
(1)饮料中的一种酸是___________;
(2)用于改良酸性土壤的碱是 ;
(3)农业生产中用作复合肥的盐是________。
下列数据是硝酸钾固体在不同温度时的溶解度。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
| 溶解度/g |
13.3 |
31.6 |
63.9 |
110 |
169 |
(1)硝酸钾溶液中的溶剂是。
(2)20℃时,向100 g水中加入31.6 g硝酸钾,充分溶解后得到(填“饱和”或“不饱和”)溶液。
(3)20℃时,向100 g水中加入40 g硝酸钾,若使硝酸钾完全溶解,可采用的方法是。
(4)如图,小烧杯中盛放的是(2)中所得的硝酸钾溶液。若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是(填字母)
A.冰 B.浓硫酸 C.硝酸铵 D.干冰 E.氢氧化钠 F.氧化钙
(5)向一定量饱和的石灰水中加入少量的生石灰恢复到原温度,产生的现象是;其中改变的量是。(提示:CaO+H2O→Ca(OH)2 )
A.溶质的质量B.溶剂的质量 C.溶液的质量 D.溶质的质量分数
形象的微观示意图有助于我们认识化学物质和理解化学反应。
(1)若用 表示氧原子,用
表示氧原子,用 表示氢原子。
表示氢原子。
则 表示,
表示,
 表示,
表示,  表示。(填化学符号)
表示。(填化学符号)
(2)在点燃条件下,A和B反应生成C和D。反应前后分子种类变化的微观示意图如下
所示。
请回答以下问题:
①1个B分子中含有_____个原子。
②A中氮元素和氢元素的质量比为_____。
③4种物质中,属于化合物的是_____(填图中字母)。
④在该反应中,生成C和D的质量比为_____(计算结果用最简整数比表示)
水是重要的自然资源。
(1)下图所示的3个实验,A中水发生了______(填“物理”或“化学”)变化;B中试管2内得到的气体为________;C中净化水的方法是______和吸附。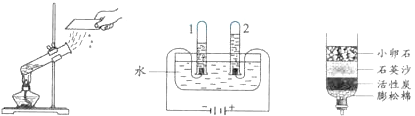
A.水的沸腾 B.水的电解 C.水的净化
(2)北京市为严重缺水城市,下列做法中,可能会造成水污染的是。
A.生活污水经集中处理后排放 B.禁止用含磷洗涤剂
C.在水库周边兴建造纸厂 D.实施对农药和化肥使用监控
(3)“84消毒液”可用于灾区防疫。制备其主要成分次氯酸钠(NaClO)的化学方程式为;2NaOH + Cl2="=" NaClO +NaCl+X,则X的化学式为;
化学知识在生活中到处可见。
(1)合理搭配饮食是我们的健康理念。比如早餐搭配:牛奶、面包、黄油、水果等,其中含有的营养素有油脂、糖类、蛋白质、维生素、无机盐和。
(2)下图所示常见用品中,属于有机合成材料的是 (填字母)。根据图A推断金属具有的性质是__________________。
(3)当人体内缺钙时,可能患有的疾病是。
A.食欲不振 B.骨质疏松 C.夜盲症D.贫血病
(4)煤、和 天然气常称为化石燃料。
(5)下列日常生活中的做法,符合“低碳生活”理念的是________。
A.节约使用纸张 B.分类回收处理垃圾
C.减少使用塑料袋 D.减少使用一次性纸杯
在化学世界中,呆板的的阿拉伯数字变得鲜活起来,请把下列化学符号中数字“2” 所表示的意义,将其序号填在相应的横线上:(每空1分,共4分)
所表示的意义,将其序号填在相应的横线上:(每空1分,共4分)
(1).Fe2+ (2).NO2 (3).2NO(4).  O
O
(1), (2);
(3) ,(4)。
,(4)。