今年地球日主题为:“珍惜地球资源,转变发展方式”。为减少化石燃料的使用,降低污染,各国都在积极进行技术创新。
(1)美国科学家发明了一种“发电叶子”,将这种叶子放入水中,在太阳光照射下,叶子中的催化剂会将水分解成氢气和氧气储存在氢氧燃料电池中,再转化为电能,供家庭用电需求。
①整个过程中都发生了哪些形式的能量转化: 。
②“发电叶子”产生氢气、氧气的化学方程式为 。
(2)我国积极改进风电技术,扩大风电使用,并配套大型储能设备——“全钒液流”储能电池,以保证稳定供电。
①与煤炭火力发电相比,风力发电的优点是 。
②“全钒液流”储能电池在充电时,电池中的VO2+会变成VO2+,这个过程中钒元素(V)的化合价由 价变为 价。
(3)为了降低汽车排放的尾气对空气的污染,现在的大部分汽车都安装了催化式排气净化器。下图列举的是几种气体在净化器中转换前后的变化。
①根据下图所提供的信息,举例说明催化式排气净化器是如何降低汽车尾气污染的:
。
②气体在催化式排气净化器里面发生了化学变化。请用原子、分子的知识概括化学变化的实质: 。
③为了使汽车尾气的污染更小,研究催化式排气净化器的专家们还要注意什么问题:
。
化学课上,老师向盛有少量碳酸钠溶液的试管中加入一定量的澄清石灰水,出现了白色沉淀,反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。据此现象,老师提出如下问题,请回答:
(1)反应后溶液中溶质是什么?
小明认为有以下四种情况,请你替他补充完整:
情况①:
情况②:NaOH和Na2CO3
情况③:NaOH和Ca(OH)2
情况④:NaOH、Na2CO3和Ca(OH)2
小红认为只有三种情况,其中情况(填序号)不可能,理由是。
(2)为了进一步确定反应后溶液的成分,小强设计了如下实验方案:
实验步骤 |
实验现象 |
实验结论 |
| 取少量溶液于试管中,滴加过量稀盐酸 |
无明显现象 |
情况(填序号)不可能 |
| 另取少量溶液于试管中,加入 |
情况③正确 |
同学们的回答,得到了老师满意的赞赏。
某研究型学习小组的同学在用浓硫酸处理废锌片时发现产生的气体具有刺激性气味,这种现象引起同学们的思考和研究。
【提出猜想】对产生的气体进行猜想:
猜想1:可能是H2;
猜想2:可能是SO2;
猜想3:可能是
【查阅资料】SO2易溶于水,能与NaOH溶液反应生成Na2SO3。
【实验方案】研究性学习小组的同学设计如图所示的装置进行研究(夹持仪器已省略,假设装置中的反应都进行完全)。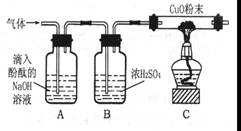
【问题讨论】
(1)如果装置A中没有明显现象,装置C中的现象为则猜想成立。
(2)如果装置A中的现象为,装置C中没有明显的现象则猜想成立。
(3)猜想3成立的实验现象是
。
(4)装置B中浓硫酸的作用是。
【思维拓展】
实验室中可以用氢氧化钠溶液吸收二氧化硫,反应的化学方程式是
。
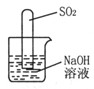
(2)小组内一同学又设计了判断SO2与NaOH溶液能否反应的装置(如图),实验时发现试管内液面上升,就得出SO2与NaOH溶液反应的结论,其同学认为这一结论不严谨,理由是。要得到科学严谨的结论,仍利用该装置,需做的对比实验是
。
(1)实验室给你提供了下列仪器,请选用合适的仪器完成指定的实验。

①要制取较多的O2用来探究其性质(要求制取过程中可以添加反应物),组装气体发生装置需要的仪器是___ ___(填序号),收集氧气应采取___ _____法。
②提纯粗盐时,过滤需要选用上述仪器中的_____ ____(填序号),除此之外还缺少的仪器是____ _____、____ ______(填名称)。
(2)美羊羊同学在购买回的袋装薯片中发现还有一个小袋,上面标有“成分:CaO、Fe;作用:防潮、防氧化;警告:禁止食用”等字样,撕开小袋,发现里面的固体粉末有少许是棕红色的,大多数是灰白色的。经过分析,她认为棕红色粉末是Fe2O3,灰白色粉末应该含有CaCO3和Fe,为验证自己的判断,美羊羊同学打算进行实验探究,请你一同参与。
【实验目的】证实灰白色粉末中含有CaCO3和Fe。
【实验设计】装置如下图所示:

【实验预测与分析】
①若要证实样品中含有CaCO3,观察到的实验现象是_______ ____________,B中发生反应的化学方程式为___ _____。
②若要证实样品中含有Fe,E中应观察到的现象是____ _________,此时C装置的作用是____ ____________。
③看了美羊羊同学的分析结论,有同学认为小袋内灰白色粉末中还应该有别的物质,请你写出其中一种物质的化学式__________。
通过学习碱的性质,我校化学兴趣小组的同学对实验室的“氢氧化钙是否变质以及变持的程度”展开了探究活动,请你一同参与:
⑴提出问题:氢氧化钙是否变质?
⑵猜想与假设:同学们经过讨论认为样品存在三种可能情况:没有变质;部分变质;完全变质。
⑶实验探究:
| 实验步骤及操作 |
实验现象 |
实验结论 |
| 取样于试管中,加入足量蒸馏水振荡,静置 ①取上层清液,滴入无色酚酞试液 ②倒去上层清液,再向试管中注入稀盐酸 |
①无色酚酞试液变红 ② |
部分变质 |
| ①无色酚酞试液不变红 ② |
||
| ① ②没有气泡产生 |
⑷小结与思考:
①小蔓同学根据上述实验方案进行实验,确定该样品已部分变质,请写出实验中反应的化学方程式:
②氢氧化钙俗称熟石灰,农业上常用来。
某兴趣小组的同学们以“稀硫酸与氢氧化钠溶液能否发生反应”为课题进行了科学探究。
同学们在烧杯中加入10mL稀硫酸。滴入几滴酚酞试液,接着分两次向烧杯中滴入氢氧化钠溶液。第一次滴加几滴氢氧化钠溶液后,不断搅拌,第二次继续滴加氢氧化钠溶液至过量。则第一次滴加氢氧化钠溶液时,溶液中溶质(不考虑酚酞)的质量变化情况是__________:第二次滴加氢氧化钠溶液时观察到的现象是_______________________。
由上述实验同学们得出了稀硫酸与氢氧化钠溶液能发生反应的结论。
[提出问题]是否可以用其他试剂证明稀硫酸与氢氧化钠溶液能发生反应呢?
[甲组实验]实验过程如图所示:
现象:向a试管中滴加氢氧化钠溶液时无明显现象,再滴加几滴硫酸铜溶液时出现蓝色沉淀。
结论:用硫酸铜溶液可以证明稀硫酸与氢氧化钠溶液能发生反应。
[乙组实验]实验过程如图所示:
现象:向b试管中滴加氢氧化钠溶液时无明显现象,再滴加几滴氯化钡溶液时出现白色沉淀。
结论:用氯化钡溶液可以证明稀硫酸与氢氧化钠溶液能发生反应。
[交流评价]请你评价甲、乙两组同学由实验现象获得的结论是否正确,并说明理由。
| 正确或错误 |
理由 |
|
| 甲组 |
||
| 乙组 |