(12分)请写出下列有机物的官能团。
CH3CH2CH2COOH , HCOOC2H5 ,
CH3CH2CH2CH2-Cl , CH3CHO ,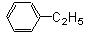 ,
,  ,
,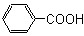 , CH3CH2CH=CHCH3 ,
, CH3CH2CH=CHCH3 ,
化学中的某些元素是与生命活动密不可分的元素,请回答下列问题。
(1)维生素C是一种水溶性维生素,水果和蔬菜中含量丰富,该物质结构简式如图所示。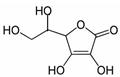
①维生素C分子中碳原子的杂化方式有。
②1 mol维生素C分子中含有mol π键。
③维生素C分子中所含元素电负性由大到小的顺序为。
④维生素C晶体溶于水的过程中要克服的微粒间作用力有。
(2)KSCN溶液可用于Fe3+的检验,原因是铁离子外围有较多能量相近的空轨道,因此能与一些分子或离子形成配合物。Fe3+的价电子排布为,与之形成配合物的分子或离子中的配位原子应具备的结构特征是。
(3)Fe3O4具有反尖晶石结构。某化合物MgxAlyOz与反尖晶石结构相仿,其结构如下图所示,它是由下列A、B方块组成。该化合物的化学式为________。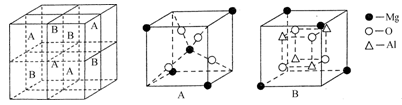
(选做)铜是过渡金属元素,可以形成多种化合物。
(1)铜基态原子的核外电子排布式为。
(2)Cu+与NH3形成的配合物可表示成[Cu(NH3)n]+,该配合物中,Cu+的4s轨道及4p通过sp杂化接受NH3提供的电子对。
[Cu(NH3)n]+中Cu+与n个氮原子的空间结构呈,n=。
(3)CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(en)2]2+(en是乙二胺的简写):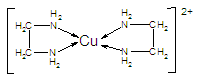
请回答下列问题:
①乙二胺分子中氮原子轨道的杂化类型为。
②配合物[Cu(en)2]Cl2中属于第二周期且第一电离能从大到小排列的是。
③乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是。
④配合物[Cu(en)2]Cl2中不存在的作用力类型有(填字母)。
| A.配位键 |
| B.极性键 |
| C.离子键 |
| D.非极性键 |
E.氢键
F.金属键
(4)向氯化铜溶液中通入足量的二氧化硫,生成白色沉淀M,M的结构单元如图所示。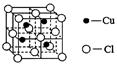
写出该反应的离子方程式__________________。
高锰酸钾是强氧化剂,它的用途遍布各个行业。
(1)工业上由软锰矿(主要成分为MnO2)生产髙锰酸钾分为两个步骤:
①步骤一将软锰矿与过量的固体KOH和空气在高温下反应,生成锰酸钾(K2MnO4),该反应的化学方程式是。
②步骤二以石墨为阳极,铁为阴极,电解锰酸钾(K2MnO4)溶液,在(填“阴极区”或“阳极区”)得到高锰酸钾。阴极反应的电极反应式是。
(2)某研究小组用工业生产高锰酸钾产生的废渣——锰泥(含K2MnO4、MnO2及Pb、Ca等元素)和乳钢废酸液制取工业级碳酸锰(MnCO3),其流程如下: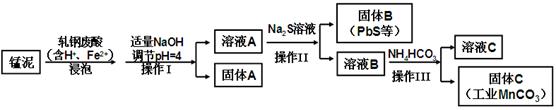
③轧钢废酸中Fe2+的作用是。
④操作I、操作Ⅱ、操作Ⅲ的名称是。
⑤溶液C中除含有Ca2+、Mn2+、H+外,还含有的阳离子是。
⑥若固体C中不含CaCO3,则溶液C中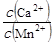 <(已知:Ksp(MnCO3)=1×10-11,Ksp(CaCO3)=5×10-9)。
<(已知:Ksp(MnCO3)=1×10-11,Ksp(CaCO3)=5×10-9)。
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:元素W的一种原子的原子核中没有中子;元素X 构成的某种单质在自然界中硬度最大;元素Z在地壳中含量最高。试回答下列各题:
(1)元素Z在周期表中的位置为。
(2)由W、X、Z三种元素可组成A、B、C三种常见的有机化合物,其中A和B是日常生活中常用调味品的主要成分,且A与B能够反应生成C,写出该反应的化学方程式。
(3)由W、X、Y、Z四种元素中的三种元素组成中学化学常见的某种化合物,其浓溶液可与其中第四种元素的单质发生反应,写出该反应的化学方程式:。
(4)W、Y、Z可组成离子化合物M,M的水溶液呈(填“酸性”或“碱性”或“中性”),M溶液中各离子浓度由大到小的顺序为;W、Y、Z也可组成共价化合物N,M和N两种溶液的pH均为a,那么两溶液中由水电离出的c (H+)的比为。
(5)已知由元素X和Z可组成A、B、C、D四种中学化学常见的单质或化合物,四种物质之间存在如图所示的转化关系。
已知:298K时,反应①生成1mol B(g)时放出393.5 kJ热量,反应④生成1mol B(g)时放出283.0 kJ的热量,反应③的热化学方程式为。
I.短周期元素X、Y、Z在元素周期表中的位置如下图所示,其中Y元素原子的最外层电子数是电子层数的两倍。回答下列问题: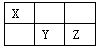
(1)Y元素在元素周期表中的位置是。
(2)列举一个事实证明Y元素与Z元素的非金属性强弱:。
(3)X的气态氢化物与其最高价氧化物对应的水化物反应生成盐。该盐溶液的pH7(填“<”、“>”或“=”),其原因为(用离子方程式表示)。
(4)X元素的某种液态氢化物,分子中含有18个电子,只存在共价单键。该物质在碱性溶液中能够将CuO还原为Cu2O,同时生成一种参与大气循环的气体。该反应的化学方程式为。
II.已知可逆反应:CO(g)+H2O(g) 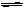 CO2(g)+H2(g),平衡常数见下表:
CO2(g)+H2(g),平衡常数见下表:
| 温度/℃ |
500 |
700 |
850 |
1 000 |
| 平衡常数 |
2.5 |
1.7 |
1.0 |
0.6 |
(5)该反应ΔH0(填“<”或“>”)。
(6)850 ℃时,若向一容积固定的密闭容器中同时充入1.0 mol CO、3.0 mol H2O、1.0 molCO2和x mol H2,若要使上述反应开始时正向进行,则x应满足的条件是。
若x=5.0,当反应达到平衡时,n(H2)=。