如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+ 2B(g) C(g)
C(g) +2D(g);ΔH<0达到平衡(Ⅰ)时,V(乙)="0.86V" L。请回答:
+2D(g);ΔH<0达到平衡(Ⅰ)时,V(乙)="0.86V" L。请回答: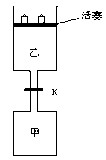
(1)乙中B的转化率为 ;
(2)甲中D和乙中C的物质的量比较: (填“相等”、“前者大”、“后者大”);
(3)打开K,过一段时间重新达平衡(Ⅱ)时,乙的体积为 (用含V的代数式表示,连通管中气体体积忽略不计)。
工业上可由有机化工原料A或E制得橡胶M,它是理想的电线电缆材料,其合成路线如下图所示。(二聚指两个相同的分子聚合为一个分子的过程,三聚、四聚同理)
完成下列填空:
A的名称是
(2)写出反应②的化学反应方程式 。
(3)写出将E三聚成环状化合物的结构简式 。
(4)以下是由A制备工程塑料PB的原料之一1,4-丁二醇(BDO)的合成路线:
|

|
写出上述由A制备BDO过程中反应⑤的化学反应方程式。
制造导弹的雷达罩和宇航员使用的氧气瓶的主要材料是透明聚酯玻璃钢,制备它的一种配方中含有下列四种物质:



(甲) (乙) (丙) (丁)
填写下列空白:
(1)甲中不含氧原子的官能团是______;甲分子_____(填“有”或“无”)顺反异构现象;下列试剂能与甲反应而褪色的是(填标号)。
a. Br2/CCl4溶液 b. 石蕊溶液 c.酸性KMnO4溶液
(2)写出乙与足量Na反应的化学方程式。
(3)已知:
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是 。
(4)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与FeCl3溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为 。
实验室制备溴代烃的反应如下:NaBr+H2SO4==HBr+NaHSO4①
R-OH+HBr R-Br+H2O②
R-Br+H2O②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下;
| 乙醇 |
溴乙烷 |
正丁醇 |
1-溴丁烷 |
|
| 密度/g·cm-3 |
0.7893 |
1.4604 |
0.8098 |
1.2758 |
| 沸点/℃ |
78.5 |
38.4 |
117.2 |
101.6 |
请回答下列问题:
(1)在溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是。
a.圆底烧瓶b.容量瓶c.锥形瓶d.量筒
(2)溴代烃的水溶性(填“大于”、“等于”或“小于”)相应的醇;其原因是。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在(填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的不正确的是。
a.水是反应的催化剂b.减少Br2的生成
c.减少HBr的挥发d.减少副产物烯和醚的生成
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其原因是;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是。
含苯环的化合物A,相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为;
(2)A与溴的四氯化碳溶液反应的化学方程式为;
(3)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式;
(4)在一定条件下,由A聚合得到的高分子化合物的结构简式为。
(5)B是A 的一种同分异构体,且B的一氯代物只有一种,则B的结构简式是。
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
(1)D元素位于第周期第族。
(2)元素B、G、J、K、D的原子半径由大到小的顺序是(用元素符号表示)。
(3)K、G两种元素的最高价氧化物对应的水化物能发生反应,请写出该反应的化学方程式:。
(4)DA3、CE2、AK三种分子中,分子内所有原子都达到8电子稳定结构的分子为:(用化学式表示)。