根据元素周期律和周期表回答下列问题:
⑴短周期中,金属性最强的元素是 ,非金属性最强的元素是 ;非金属元素共 种(稀有气体除外)(用化学用语回答,下同)。
⑵第3周期中,原子半径最小的元素(稀有气体元素除外)是 ,简单的离子半径最小的是 ,非金属性最强的元素是 ;
(3)周期表中位于第8纵列的铁元素属于第 周期第 族。周期表中最活泼的非金属元素位于第 纵行。
有A、B两位学生均想利用原电池反应验证金属的活动性顺序,并探究产物的有关性质,分别设计了如图所示的原电池,请完成下列问题: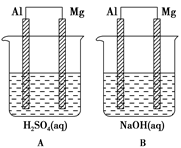
(1)①负极材料:
A池________,B池________。
②电极反应式:
A池:正极:________,负极:________
B池:正极:________,负极:________
(2)B池总反应的离子方程式为_________________________________。
如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地往烧杯中央滴入CuSO4溶液。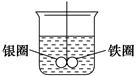
(1)片刻后可观察到的现象是(指悬吊的金属圈)________。
| A.铁圈和银圈左右摇摆不定 |
| B.保持平衡状态不变 |
| C.铁圈向下倾斜 |
| D.银圈向下倾斜 |
(2)产生上述现象的原因是________________________________________。
(3)写出反应的化学方程式:______________________________________。
在一个小烧杯里加入约20 g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10 g氯化铵晶体,并立即用玻璃棒迅速搅拌。试回答下列问题:
(1)写出反应的化学方程式: _____________________________。
(2)实验中要立即用玻璃棒迅速搅拌的原因是_____________________________。
(3)如果实验中没有看到“结冰”现象,可能的原因是(答出三个或三个以上原因)__________________________ _____________。
(4)如果没有看到“结冰”现象,我们还可以采取哪些方式来说明该反应吸热?
_______________________________________(答出两种方案)。
(5)“结冰”现象说明该反应是一个________(填“放出”或“吸收”)能量的反应。即断开旧化学键________(填“吸收”或“放出”)的能量________(填“>”或“<”)形成新化学键________(填“吸收”或“放出”)的能量。
(6)该反应在常温下就可进行,说明_________________________________。
已知化学反应N2+3H2 2NH3的能量变化如图所示,
2NH3的能量变化如图所示,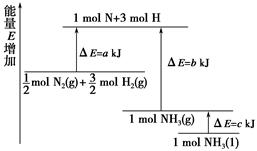
(1)1 mol N和3 mol H生成1 mol NH3(g)是________能量的过程(填“吸收”或“释放”)。
(2)由 mol N2(g)和
mol N2(g)和 mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)________kJ能量。
mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)________kJ能量。
如图所示,把试管小心地放入盛有(20 ℃)碳酸饮料的烧杯中,试管中开始放入适量饱和CuSO4溶液,再用滴管滴加5 mL浓硫酸于试管中,试回答下列问题:
(1)实验中观察到的现象是________________。
(2)产生上述现象的原因是________________。
(3)试管中破坏化学键的类型是______________,形成的化学键类型是______________。
(4)写出有关现象的化学方程式______________。
(5)由实验推知,反应所得溶液的总能量__________(填“大于”、“小于”或“等于”)浓硫酸和饱和CuSO4溶液的总能量。