(3分)下图是一氧化碳燃烧的微观模拟图,请回答下列问题:
(1)此变化过程中,发生变化的粒子是___________________________
(2)对此变化的实质从微观角度的解释是___________________________
2022年2月4日至20日,北京成功举办第24届冬季奥运会。
(1)本届冬奥会的吉祥物“冰墩墩”的冰晶外壳由塑料制成,该外壳材料属于 (写“复合材料”或“合成材料”)。
(2)本届冬奥会期间提供的各种具有中国特色的美食,受到各国运动员的欢迎,尤其以烤鸭、牛肉水饺更受青睐。这两种美食中都富含的营养素是 (写一种)。
(3)“低碳”是本届冬奥会的主题,其速滑馆“冰丝带”采用了当前最环保的技术——二氧化碳跨临界直冷制冰技术。该技术的过程之一,就是通过压力将二氧化碳由气态直接转化为固态。这个过程从微观角度看,未发生改变的是 。
安全的家居环境和健康的饮食会使生活更美好。
(1)水基型灭火器是家庭常备灭火器,灭火时产生的泡沫喷射在可燃物表面形成一层水膜使火熄灭。其灭火原理是 。
(2)为预防碘缺乏症,国家规定缺碘地区食用加碘盐,即在食盐中添加适量的 。 中碘元素的化合价是 。
(3)某同学的午餐食谱为炖羊肉、红烧鱼、炒青椒、鲜牛奶和新鲜果蔬。从合理膳食的角度考虑,建议应增加的食物是 。
“碳中和”是指通过植树造林、节能减排、碳捕集与封存等形式,抵消生产生活中产生的 ,从而达到 相对“零排放”。
回答下列问题:
(1)“碳中和”的“碳”是指 。
(2)化石燃料的过度使用会加剧的环境问题是 。
(3)转化法是实现“碳中和”的措施之一,将 和 在催化剂的作用下转化成甲醇( )和水是目前研究的热点。写出该反应的化学方程式 。
(4)在日常生活中,你如何践行“碳中和”理念(写一条即可) 。
水及溶液在生产、生活中有着广泛的用途。
(1)将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为 (填序号)。
①蒸馏②加明矾吸附沉降③杀菌④蒸发⑤过滤
(2)用固体配制一定溶质质量分数的溶液时用到的玻璃仪器有广口瓶、烧杯、量筒、 、胶头滴管和细口瓶。
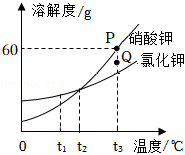
(3)硝酸钾和氯化钾两种固体物质的溶解度曲线如图所示,请回答下列问题:
① 时,用等质量的硝酸钾和氯化钾配制饱和溶液,需要水的质量关系为:前者 (填“>”“<”或“=”)后者。
② 时,硝酸钾饱和溶液的溶质质量分数为 。
③根据图中信息判断,以下说法正确的有 (填字母序号)。
| A. |
时,硝酸钾和氯化钾溶解度相等 |
| B. |
若使硝酸钾溶液的状态由P点变为Q点,只可采用加水的方法 |
| C. |
时,氯化钾的饱和溶液升温至 ,溶质质量不变 |
| D. |
将 时硝酸钾和氯化钾的饱和溶液冷却至 ,析出晶体质量的大小关系为硝酸钾大于氯化钾 |
阅读下列短文并回答问题。
国家卫健委公布的《新型冠状病毒肺炎诊疗方案(试行第九版)》中提到:新型冠状病毒对紫外线和热敏感,56℃30分钟、乙醚、75%乙醇、含氯消毒剂(如二氧化氯、“84”消毒液)等均可有效灭活病毒。其主要的传播途径为经呼吸道飞沫和密切接触传播。在相对封闭的环境中经气溶胶传播。接触被病毒污染的物品后也可造成感染。接种新型冠状病毒疫苗是降低重症和减少死亡发生率的有效手段。新型冠状病毒的一般预防措施有保持良好的个人及环境卫生,均衡营养、适量运动、充足休息,提高健康素养,科学做好个人防护……
(1)消毒剂二氧化氯的化学式是 ,其中氯氧元素质量比为 (填最简整数比)。
(2)“84”消毒液的有效成分 可通过反应 制得,化学方程式中X的化学式为 , 中氯元素的化合价为 。
(3)化学知识在新型冠状病毒肺炎疫情防控中发挥着重要作用。下列说法正确的是 (填字母序号)。
| A. |
打喷嚏或咳嗽时应掩住口鼻 |
| B. |
使用医用酒精时应远离火源 |
| C. |
勤洗手、戴口罩是防止病毒入侵的有效方法 |
| D. |
95%的酒精溶液的消毒能力比75%的酒精溶液强 |
(4)疫情期间要均衡饮食,保证健康。以下食物中富含维生素的是 (填字母序号)。
| A. |
馒头 |
| B. |
烤羊排 |
| C. |
凉拌黄瓜 |
| D. |
煎带鱼 |
| E. |
柠檬汁 |