已知:4NH3(g)+5O2(g)=4NO(g)+6H2(g);△H=-1025kJ/mol该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是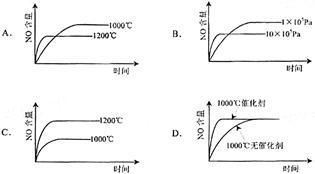
若ABn的中心原子A上没有未用于形成共价键的孤电子对,运用价层电子对互斥理论,判断下列说法中正确的是
| A.若n=2,则分子的立体结构为V形 |
| B.若n=3,则分子的立体结构为三角锥形 |
| C.若n=4,则分子的立体结构为正四面体形 |
| D.以上说法都不正确 |
实验测得CO2为共价化合物,两个C=O键间的夹角为180°,以下判断正确的是
| A.由极性键构成的极性分子 | B.由极性键构成的非极性分子 |
| C.由非极性键构成的极性分子 | D.CO2中C采取sp2杂化 |
下列分子中所有原子都满足最外层8电子结构的是
①SF6②PCl5 ③PCl3④CS2 ⑤NO2 ⑥N2
| A.①②④⑤ | B.②③⑤⑥ | C.③④⑥ | D.①③⑤ |
中学化学中很多“规律”都有其使用范围,下列根据有关“规律”推出的结论合理的是
| A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 |
| B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| C.根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性 |
| D.根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是
| A.直线形;三角锥形 | B.V形;三角锥形 |
| C.直线形;平面三角形 | D.V形;平面三角形 |