(1)某温度下,纯水中c(H+) = 5×10-7 mol·L-1,则此时纯水中的c(OH-) =" ____" mol·L-1;若温度不变,滴入稀硫酸使c(H+) = 5.0×10-3 mol·L-1,则c(OH-) =" ____" mol·L-1。
(2)已知室温下pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液呈酸性,则高碘酸的电离方程式是__________________________。
将4 mol SO3气和4 molNO置于2L容器中,一定条件下发生如下可逆反应(不考虑NO2和N2O4之间的相互转化):2SO3(g)  2SO2+O22NO+O2
2SO2+O22NO+O2 2NO2
2NO2
(1)当上述系统达到平衡时,O2和NO2的物质的量分别为n(O2)="0.1" mol、n(NO2)="3.6" mol,则此时SO3气的物质的量为 。
(2)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是SO3和,或NO和(填它们的分子式)。
反应aA(g)+bB(g) cC(g)(
cC(g)(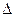 H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示: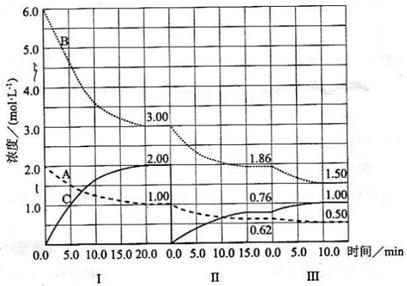
回答问题 :
:
(1)反应的化学方程式中,a:b:c为;
(2)B的平衡转化率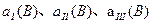 中最小的是,其值是;
中最小的是,其值是;
(3)由第一次平衡到第二次平衡,平衡移动的方向是,采取的措施是;
(4)比较第II阶段反应温度(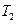 )和第III阶段反应速度(
)和第III阶段反应速度(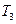 )的高低:
)的高低: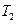
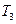 填“>、=、<”判断的理由是。
填“>、=、<”判断的理由是。
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。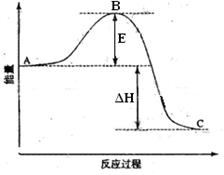
已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题: (1)图中A表示
(1)图中A表示 ,图中△H=KJ·mol-1;
,图中△H=KJ·mol-1; (2)该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?,V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式;
(2)该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?,V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式; (3)已知单质硫的燃烧热为296 KJ·mol-1,求由S(s)生成1 molSO3(g)的△H=
(3)已知单质硫的燃烧热为296 KJ·mol-1,求由S(s)生成1 molSO3(g)的△H=
现有①汽车②机器上的齿轮③门把手④锯条⑤铁洗脸盆等常见铁制品。为了防止它们生锈,通常适合采用下面哪一种方法。(填序号)
(1)在表面喷漆_________;(2)在表面涂油_________;(3)在表面镀一层其他金属_________;(4)在表面烧制搪瓷_________;(5)使其表面形成致密的氧化物保护膜_________;(6)制成不易生锈的合金不锈钢_________;
近年来,为满足某些尖端技术的发展需要,人们又设计和合成了许多新型合金材料。如:储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料。此外, 、、和等新型合金广泛应用于卫星、航空航天、生物工程和电子工程等领域。
、、和等新型合金广泛应用于卫星、航空航天、生物工程和电子工程等领域。