一定条件下,在一容积可变的密闭容器中,反应: 过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表: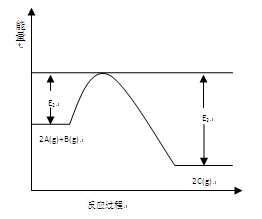
| 时间(min) |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
| n(A) |
2.00 |
1.90 |
1.82 |
1.76 |
1.64 |
1.54 |
1.50 |
1.50 |
1.50 |
| n(B) |
1.00 |
0.95 |
0.91 |
0.88 |
0.82 |
0.77 |
0.75 |
0.75 |
0.75 |
| n(C) |
0 |
0.10 |
0.18 |
0.24 |
0.36 |
0.46 |
0.50 |
0.50 |
0.50 |
回答下列问题:
(1)反应 的正反应△H (填“大于”或“小于”)0。
的正反应△H (填“大于”或“小于”)0。
(2)该反应平衡时,下列说法不正确的是
(A)气体的密度不再改变 (B)A的物质的量浓度不变
(C)放出或吸收的热量不再变化 (D)v正(A)=v逆(A)=0
(3)toC时,在一容积为2L的恒容密闭容器内加入0.4molA和0.6molB,在一定条件下发生反应,反应中C的物质的量浓度变化情况如下图: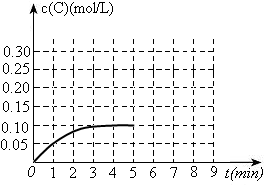
①该温度下,反应: 的平衡常数K= 。
的平衡常数K= 。
②反应进行到1分钟时B物质的量为 。
③在第5min时,将容器的体积缩小一半后,若在第8min达到新的平衡时A的总转化率为75%,请在上图中画出第5min到新平衡时C的物质的量浓度的变化曲线。
有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液的实验如下:
| 实验步骤 |
实验现象 |
| (1)取少量该溶液,加几滴甲基橙 |
溶液变红色 |
| (2)取少量该溶液加热浓缩,加Cu片和浓硫酸,加热 |
有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 |
有白色沉淀生成 |
| (4)取(3)中的上层清夜,加AgNO3 |
有稳定的白色沉淀生成,且不溶于稀硝酸 |
| (5)取少量该溶液,加入NaOH溶液 |
有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
由此判断:
(1)溶液中一定存在的离子是__________;溶液中肯定不存在的离子是:____________
(2)写出(3)步的离子方程式: ___________________________________
(3)写出(5)步沉淀部分溶解的离子方程式: ___________________________________
某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是。
(2)该反应中,发生还原反应的过程是→。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目
。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为。
短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。请回答:
(1)Y元素的名称是。
(2)XZ3化合物的电子式是______________ 分子的立体构型
(3)分别写出X、Y的最高价含氧酸的分子式、。





















 苯酚是重要的化工原料,通过下列流程可合成阿司匹林、香料和一些高分子化合物。已知:
苯酚是重要的化工原料,通过下列流程可合成阿司匹林、香料和一些高分子化合物。已知:
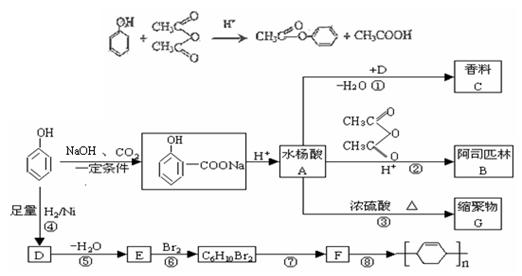










 (1)写出反应类型:④__________________,⑦_________________。
(1)写出反应类型:④__________________,⑦_________________。 (2)写出浓硫酸催化条件下,香料C的结构简式____________________,
(2)写出浓硫酸催化条件下,香料C的结构简式____________________, G的结构简式_____________________。
G的结构简式_____________________。 (3)写出反应②的化学方程式_________________________________。
(3)写出反应②的化学方程式_________________________________。 (4)写出反应⑧的化学方程式_____________________________________。
(4)写出反应⑧的化学方程式_____________________________________。 (5)下列可检验阿司匹林样品中混有水杨酸的试剂是__
(5)下列可检验阿司匹林样品中混有水杨酸的试剂是__ ________。
________。 (a)三氯化铁溶液(b)碳酸氢钠溶液(c)石蕊试液
(a)三氯化铁溶液(b)碳酸氢钠溶液(c)石蕊试液
(1).CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为,与CO互为等电子体的离子为 (填化学式)。
(2).人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”。Ti 元素在元素周期表中的位置是周期,第族;其基态原子的价电子层排布为;
(3). 在Ti的化合物中,可以呈现+2、+3、+4 三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如图,它的化学式是;
(4)已知Ti3+可形成配位数为6的配合物。现有含钛的两种颜色的晶体,一种为紫色,另一为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a. 分别取等质量的两种配合物晶体的样品配成待测溶液;
b. 分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c. 沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的 。
。
则绿色晶体配合物的化学式为,绿色晶体中含有化学键类型是。