现有部分短周期元素的原子结构如下表:
| 元素编号 |
元素原子结构 |
| X |
原子结构示意图为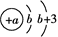 |
| Y |
最外层电子数是次外层电子数的2倍 |
| Z |
原子核内含有12个中子,且其离子的结构示意图为 |
(1)写出X的元素符号:____________,Z元素原子的质量数为________。
(2)元素Y的最高价氧化物的结构式为______________, Z元素的单质在空气中燃烧产物的电子式_________,用电子式表示X的气态氢化物的形成过程 。
(3)Y的最高价氧化物和Z元素的单质在空气中燃烧产物发生反应的化学方程式为 ;若反应过程中,转移电子数为6.02×1023,则消耗Y的最高价氧化物的质量为 。
(8分)四种短周期非金属元素A、B、C、D,原子序数依次增大。A是原子半径最小的元素,B原子的最外层电子数是次外层电子数的两倍,D在地壳中含量最大。请回答:
(1)B元素的原子结构示意图是。
(2)化合物CA3的电子式是,BD2分子的结构式为。
(3)丙为含有上述四种元素的常见无机酸式盐,则丙的化学式为。
某些化学反应可用下式表示(未配平):A+B→C+D+H2O
请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,写出该反应的离子方程式:___________________________________________。
(2)若C为氯化钠,D是能使澄清石灰水变浑浊的无味气体,则A与B的组合是(填俗名):A________________或________________ , B______________________。
(3)若A为紫红色金属,D为无色刺激性气体,请写出符合上式的化学方程式:____________________________________________。
(4)若C、D均为气体且分子具有相同的原子个数比,则符合上式化学方程式是:____________________________________________。
(5)若A为过氧化钠,B为硫酸,则C是____________,D是_______________。
用如下图所示装置可以完成一系列实验(图中夹持装置已略去)
请回答下列问题:
I.(1)仪器p的名称是_________________,若用装置A由浓硫酸和亚硫酸钠固体制取SO2气体,并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 |
① |
② |
③ |
| 所蘸试剂 |
石蕊试液 |
品红溶液 |
碘水(黄色) |
| 现象 |
褪色 |
||
| 体现SO2的性质 |
水溶液显酸性 |
(2)写出③中反应的离子方程式_________________________________________。
II.若用装置A由浓盐酸和高锰酸钾制取Cl2气体,装置B中的四处棉花依次做了如下处理:①蘸有FeCl2溶液②蘸有淀粉KI溶液③蘸有石蕊溶液④蘸有品红溶液
(1)写出①处发生反应的离子方程式_______________________________________。
(2)在实验过程中,③处能观察到的现象___________________________________。
(3)写出装置C中“吸收多余气体”所用的试剂_______________________________
(10分) 铝是一种重要金属:
(1)生产中曾用铝热反应(铝与铁的氧化物反应生成氧化铝和铁)焊接钢轨,则铝与磁性氧化铁发生反应的化学方程式为 。该反应中氧化剂是 ,还原剂是 ,要得到1mol金属铁,需要铝的质量 g。(2) 铝与NaOH溶液反应的离子方程式为: 。在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为 。
(8分)在实验室里,某同学取一小块金属钠做与水反应的实验。试完成下列问题:
(1) 切开的金属钠暴 露在空气中,最先观察到的现象是
露在空气中,最先观察到的现象是
,所发生反应的化学方程式是 。
。
(2) 将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是:
①,②。将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是(填编号)。
| A.有气体生成 |
| B.钠融化成小球并在液面上游动 |
| C.溶液底部有银白色的金属钙生成 |
| D.溶液变浑浊 |
(3) 在钠与水反应过程中,若生成标准状况下224mL的H2,则转移的电子的物质的量为。
(4) 根据上述实验过程中钠所发生的有关变化,试说明将金属钠保存在煤油中的目的是。