Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、C1O2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + a Na2O2 = 2Na2FeO4 + b X + 2Na2SO4 + c O2↑
该反应中物质X应是 ________ ,b与c的关系是 _____________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式: ________________。
②每生成1mol FeO42-转移 _______mo1电子,若反应过程中转移了0.3mo1电子,则还原产物的物质的量为 ______ mo1。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是____________,被氧化的离子的物质的量分别是________________________。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为________________________(用含a、b的代数式表示)。
(6分)工业上常用天然气作为制备CH3OH的原料。已知:
①CH4(g)+O2(g) CO(g)+H2(g)+H2O(g) △H=-321.5 kJ/mol
CO(g)+H2(g)+H2O(g) △H=-321.5 kJ/mol
②CH4(g)+ H2O(g)  CO(g)+3H2(g) △H=+250.3 kJ/mol
CO(g)+3H2(g) △H=+250.3 kJ/mol
③CO(g)+2H2(g)  CH3OH(g) △H=-90.0 kJ/mol
CH3OH(g) △H=-90.0 kJ/mol
(1)CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为_____________。
(2)向V L恒容密闭容器中充入a mol CO与2a mol H2,在不同压强下合成甲醇。CO 的平衡转化率与温度、压强的关系如下图所示:
①压强P1____P2(填“<”、“>”或“=”)
②在100℃、P1压强时,平衡常数为________(用含a、V的代数式表示)。
写出下列反应的热化学方程式
(1)在25℃,101 Kpa 下1 mol 乙醇(C2H5OH)完全燃烧并生成二氧化碳和液态水时,放出热量为1366.8 kJ,试写出表示乙醇燃烧的热化学方程式:____
(2)肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。已知:N2(g)+2O2 (g)=2NO2(g) △H=+67.7kJ/mol
2N2H4(g)+2NO2 (g)=3N2(g)+4H2O(g)△H= 一1135.7kJ/ mol
则肼完全燃烧的热化学方程式为 。
(3)高炉炼铁中发生的基本反应之一如下:
FeO(s)+ CO(g)=" Fe(s)+" CO2(g) △H>0。
①此反应的平衡常数表达式为;
②温度升高平衡常数K值(填“增大”、“减小”、或“不变”)
③已知1100℃时,K= 0.263,此时测得高炉中c(CO2)= 0.025mol/L,c(CO)= 0.1mol/L,在这种情况下,该反应(填“是”或“不是”)处于化学平衡状态,此时化学反应速率是v正v逆(填“<”、“>”或“=”)。
(6分)请回答下列问题:
(1)在一定温度下,下列叙述是可逆反应A(g)+3B(g) 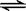 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等;
②单位时间生成amol A,同时生成3amol B;
③A、B、C的浓度不再变化;
④A、B、C的分子数目比为1:3:2 ;
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦单位时间消耗amol A,同时生成3amol B;
⑧单位时间内生成a mol C,同时生成 mol B
mol B
(2)在稀氨水中存在下述电离平衡NH3+H2O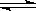 NH3 ·H2O
NH3 ·H2O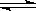 NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向移动”或“逆向移动”)
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向移动”或“逆向移动”)
| 加入的物质 |
少量NH4Cl固体 |
少量KOH溶液 |
| c(OH-)的变化 |
||
| 平衡移动方向 |
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示: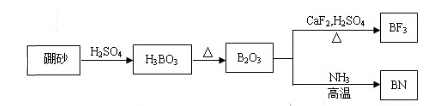
请回答下列问题:
(1)由B2O3制备BF3的化学方程式依次是_________;
(2)基态B原子的电子排布式为_________;B和N相比,电负性较大的是_________,BN中B元素的化合价为_________;
(3)在BF3分子中,B原子的杂化轨道类型为_______,BF3和过量NaF作用可生成NaBF4,BF4-的立体结构为_______;
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,立方氮化硼晶胞中含有______个氮原子、________个硼原子
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为。
②NO3- 的空间构型是(用文字描述)。
(2)在铜锰氧化物的催化下,CO 被氧化为CO2,HCHO 被氧化为CO2和H2O。
①根据等电子体原理,CO 分子的结构式为。
②H2O 分子中O 原子轨道的杂化类型为。
③1 mol CO2中含有的σ键数目为。
(3)H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:__________;
②H2SeO4比H2SeO3酸性强的原因:______;