在恒温恒容的容器中进行反应A(g)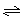 2B(g)+C(g),若A的浓度由0.1mol·L-1降到0.06mol·L-1需20s,那么由0.06 mol·L-1降到0.024 mol·L-1,需要的时间
2B(g)+C(g),若A的浓度由0.1mol·L-1降到0.06mol·L-1需20s,那么由0.06 mol·L-1降到0.024 mol·L-1,需要的时间
| A.等于18s | B.大于18s | C.等于12s | D.小于18s |
水的三态的熵值的大小关系正确的是()
| A.S (s)>S (l)>S (g) | B.S (g)>S (l)>S (s) |
| C.S (l)>S (s)>S (g) | D.S (g)>S (s)>S (l) |
下列金属防护属于电化学保护的是()
| A.改变金属内部组成结构,可以增强金属耐腐蚀的能力 | B.涂油漆 |
| C.外加电流阴极保护法 | D.在金属表面覆盖一层保护层 |
温总理在十届全国人大四次会议上所作的“政府工作报告”中指出:“抓好资源节约,建设环境友好型社会”,这是我国社会及经济长期发展的重要保证。你认为下列行为中有悖于这一保证的是()
| A.开发太阳能、水能、风能、可燃冰等新能源、减少使用煤、石油等化石燃料 |
| B.将煤进行“气化”和“液化”处理,提高煤的综合利用效率 |
| C.研究采煤、采油新技术,提高产量以满足工业生产的快速发展 |
| D.实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle) |
当反应达到平衡时,下列措施:①升温②恒压通入惰性气体,③增加 的浓度④减压⑤加催化剂⑥恒容通入惰性气体;能提高 转化率的是()
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑥ | D. | ③⑤⑥ |
关于下列各图的叙述,正确的是()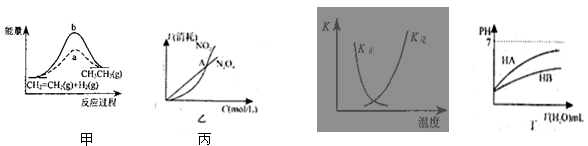
| A.图甲中a、b曲线分别表示反应CH2=CH2 (g) + H2(g)→CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化 |
B.图乙表示恒温恒容条件下发生的可逆反应2NO2(g)  N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
C.图丙中曲线表示反应2SO2(g) + O2(g)  2SO3(g);ΔH < 0 正、逆反应的平衡常数K 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化 |
| D.图丁中起始时HA的物质的量浓度大于HB |