下列反应属于放热反应的是 属于吸热反应的是 (填字母)
| A.铝片与稀H2SO4反应制取H2 | B.碳酸钙高温分解成氧化钙和二氧化碳 |
| C.葡萄糖在人体内氧化分解 | D.氢氧化钾和硫酸中和 |
E.Ba(OH)2·8H2O与NH4Cl反应
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH+6HCHO===3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤 Ⅰ 称取样品1.500 g。
步骤 Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤 Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤 Ⅲ 填空:①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积________(填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察________(填序号)。
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由________色变成________色,且半分钟内不褪色。
(2)滴定结果如下表所示:
| 滴定 次数 |
待测溶液的体积/mL |
标准溶液的体积 |
|
| 滴定前刻度/mL |
滴定后刻度/mL |
||
| 1 |
25.00 |
1.02 |
21.03 |
| 2 |
25.00 |
2.00 |
21.99 |
| 3 |
25.00 |
0.20 |
20.20 |
若NaOH标准溶液的浓度为0.1010 mol·L-1则该样品中氮的质量分数为________。
第三研究性学习小组发现某一种胃药片的制酸剂为碳酸钙,为了测定其中制酸剂的质量特制定了如下操作步骤:
①配制0.2 mol·L-1的HCl溶液和0.2 mol·L-1的NaOH溶液;②每次取一粒(药片质量均相同)0.2 g的此胃药片,磨碎后放入锥形瓶中再加入20 mL蒸馏水;③以酚酞作指示剂,用0.2 mol·L-1的NaOH溶液滴定,需用去V mL达滴定终点;④加入25 mL 0.2 mol·L-1的HCl溶液。
(1)写出全部实验过程的操作步骤的顺序:____________。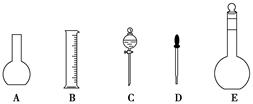
(2)上图所示的仪器中配制0.2 mol·L-1的HCl溶液和0.2 mol·L-1NaOH溶液肯定不需要的仪器是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(3)配制上述溶液应选用的容量瓶的规格分别为________(填字母)。
| A.50 mL、50 mL | B.100 mL、100 mL |
| C.100 mL、150 mL | D.250 mL、250 mL |
(4)写出相关的化学反应方程式:
________________________________________________________________________。
(5)做2次平行实验后,则每粒胃药片中含碳酸钙的质量表达式为________________g。
甲、乙两同学用一种标准盐酸去测定同一种未知浓度的NaOH溶液的浓度,但操作不同。甲把一定体积的NaOH溶液放入锥形瓶,把标准盐酸放入滴定管进行滴定;乙把一定体积的标准盐酸放入锥形瓶,把未知浓度的NaOH溶液放入滴定管进行滴定。
(1)甲使用的是________滴定管,乙使用的是________滴定管。
(2)甲同学的滴定管在用蒸馏水洗净后没有用标准盐酸润洗,乙同学的滴定管也没有用NaOH溶液润洗,其余操作均正确,这样甲测定结果偏__________,乙测定结果偏________。
氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应离子方程式是2 +
+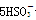 +H+===2Mn2++5
+H+===2Mn2++5 +3H2O,填空回答问题:
+3H2O,填空回答问题:
(1)该滴定实验所需仪器有下列中的________(填序号)。
| A.酸式滴定管(50 mL) | B.碱式滴定管(50 mL) |
| C.量筒(10 mL) | D.锥形瓶 |
E.铁架台 F.滴定管夹
G.烧杯 H.白纸
I.胶头滴管 J.漏斗
(2)不用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因:
________________________________________________________________________。
(3)选何种指示剂,说明理由
________________________________________________________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积偏________(填“多”或“少”)。根据(b-a) mL计算得到的待测浓度,比实际浓度偏________(填“大”或“小”)。
菠萝酯是一种具有菠萝香气的食用香料,是化合物甲与苯氧乙酸 发生化反应的产物。
发生化反应的产物。
(1)甲一定含有的官能团的名称是_____________________。
(2)5.8 g甲完全燃烧可产生0.3 mol CO2和0.3 mol H2O,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是_____________________________。
(3)苯氧乙酸有多种酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且有2种一硝基取代物的同分异构体是(写出任意2种的结构简式)___________________。
(4)已知:
菠萝酯的合成路线如下:
①试剂X不可选用的是(选填字母)____________。
a.CH3COONa溶液 b.NaOH溶液 c.NaHCO3溶液d.Na
②丙的结构简式是_________________,反应Ⅱ的反应类型是___________。
③反应Ⅳ的化学方程式是