在相同状况下,一个空瓶,若装满O2称其质量为36 g,若装满CO2称其质量为42 g,若装满A气体,称其质量为52 g,则A的相对分子质量是____________
(9分)如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。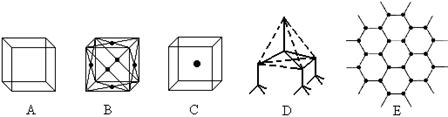
(1)其中代表金刚石的是(填编号字母,下同),其中每个碳原子与个碳原子最接近且距离相等。
(2)其中代表石墨的是,其中每个正六边形占有的碳原子平均为个。
(3)在NaCl晶体中,每个Na+周围与它最接近且距离相等的Na+有个。
(4)代表CsCl的是,它属于晶体,每个Cs+与个Cl-紧邻。
(5)干冰晶体中每个CO2分子与个CO2分子紧邻。
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应式:,负极反应式:。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:
| 氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
| Fe3+ |
1.9 |
3.2 |
| Fe2+ |
7.0 |
9.0 |
| Cu2+ |
4.7 |
6.7 |
| 提供的药品:Cl2 浓硫酸 NaOH溶液 CuO Cu |
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取两种工艺品的流程如下: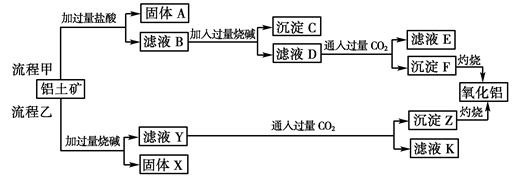
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为。
(2)流程乙加入烧碱后生成SiO32—的离子方程式为。
(3)验证滤液B含Fe3+,可取少量滤液并加入(填试剂名称)。
(4)滤液E、K中溶质的主要成份是(填化学式),写出该溶液的一种用途
。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱达到沉淀溶解平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=。
. A 、B、 C、 D、 E是中学常见的5种化合物,A 、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
(1)X的单质与A反应的化学方程式是
(2)若试剂1和试剂2均是稀硫酸。
①如何验证D中的金属离子已全部转化为E:
②物质C溶于水有净水作用,原因是:
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠
为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是
(3)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是
. 在某澄清、透明的黄色溶液中,可能含有NH4+、Fe3+、Ba2+、Al3+、SO42-、HCO3-、I-Cl-离子。进行下述实验(所加试剂均过量)。
(1) 沉淀 A的化学式是,气体A的化学式是;
(2)待测液中一定存在;一定不存在 _______用离子方程式表示上述离子一定不存在的原因。
(3)写出溶液C与过量氨水反应的离子方程式。
(4)若气体A、沉淀A、沉淀D的物质的量各为1mol,则SO42-的物质的量为: mol