物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象。某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
用pH试纸测定溶液的pH时,正确的操作是: 。
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应。
该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:NaOH溶液中滴加酚酞溶液,溶液显红色,过一会儿红色就消失了。该小组对这种意外现象的原因作如下猜想:
①可能是酚酞溶液与空气中的氧气反应,使红色消失;
②可能是NaOH溶液与空气中的二氧化碳反应,使红色消失。
(1)为了验证猜想①,该组同学做了如下实验:将配制的NaOH溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴加酚酞溶液。实验中“加热”和“滴入植物油”的目的是 。
实验结果表明酚酞溶液红色消失与空气中的氧气无关。
(2)为了验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:
结论1:说明Na2CO3溶液呈 性
结论2:说明酚酞溶液红色消失与 无关。
(3)该小组同学通过查阅资料得知:当NaOH溶液浓度很大时,就会出现上述意外现象。
请设计实验证明该方案中取用的NaOH溶液浓度过大:
①实验方案: ;
②观察到的现象 。
方案三:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。该组同学将不同浓度的盐酸和NaOH溶液各10mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后渝唐的升高值△t,(如下表)。
|
|
(1)表中x= 。
(2)某同学在没使用温度计的情况下,通过右图所示装置完成了实验。则该同学根据 判断NaOH溶液与稀盐酸发生了中和反应。
某化学兴趣小组对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。请你参与他们的探究活动,并回答有关问题。
(实验探究)(1)方案一:某同学按下图所示的方法先向试管中加入约2mL NaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为色,证明NaOH溶液与稀盐酸恰好完全反应。
①请指出下图操作中的错误。
②写出NaOH溶液与稀盐酸反应的化学方程式。
(2)方案二:
| 实验步骤 |
实验现象 |
结论 |
| 取2mL NaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 |
若 |
稀盐酸过量 |
| 若没有明显现象 |
NaOH溶液与稀盐酸恰好完全反应 |
(实验反思)(3)方案一在滴入稀盐酸的过程中,若观察到曾有少量气泡出现,请分析产生气泡的原因可能是(写出一条即可)。
(4)有同学提出方案二不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是。为此,还需要选择(填一种试剂),再进行实验即可。
(拓展应用)(5)请举一例说明中和反应在生产生活中应用。
实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3。
则NaOH变质反应的化学方程式为________________________________;
【查阅资料】
碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告。
| 实验操作 |
实验现象 |
实验结论 |
| (1)取少量样品溶于水,加入 ; |
白色沉淀产生 |
(2)该反应的化学方程式为 |
| (3)将上述反应后的混合液过滤,取滤液加入 ; |
(4) |
证明猜想Ⅱ成立。 |
某实验小组的同学用氢氧化钡溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钡溶液加入一定量稀盐酸后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想与假设】猜想一:BaCl2和Ba(OH)2;
猜想二:①;
猜想三:BaCl2和HCl.
【实验探究】实验一:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡。观察到②,得出结论:猜想一不成立;
实验二:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量,开始时有气泡产生,继续滴加一段时间后出现白色沉淀,得出结论:猜想二不成立,猜想三成立。
【表达与交流】实验二中,产生上述现象的原因是③;
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑④;
(2)要处理烧杯内的溶液,使其溶质只含有BaCl2,应向烧杯中加入过量的⑤。
(5分)小明和小霞在帮助老师整理实验室时,发现某实验台上放置一个无塞开口的细口瓶,且标签残缺,如图。对此两名同学探究溶液中溶质的成分。
[提出问题]原来开口的这瓶溶液中含一种溶质是什么(不考虑NaHCO3)?
[进行猜想]原来开口的这瓶溶液中溶质有可能是:①NaCl;②Na2CO3;③Na2SO4;④NaOH;⑤NaNO3
[进行实验]小明取样于试管中,加入足量的BaCl2溶液,看到有白色沉淀产生,再加入(1)________________,看到(2)_____________现象,证明溶液中含Na2CO3。
小霞取样于试管中,加入几滴酚酞溶液,观察到溶液变为红色,再加入过量的Ca(NO3)2,有白色沉淀产生,试管中的溶液仍然红色,说明此溶液中含有的溶质是(3)__________________。
[反思交流]通过上述两名同学的实验可知,猜想(4)__________是正确的,但实验出现上述现象的原因是(5)____________________________________________。
金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)下图是铝的原子结构示意图。下列说法不正确的是。
| A.铝原子的质子数为13 |
| B.在化合物中铝通常显+3价 |
| C.铝是地壳中含量最多的元素 |
| D.铝可作导线是由于它具有良好的导电性 |
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了下图实验,并对溶液A和固体B的成分进行了分析和实验探究。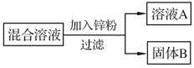
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2
②Zn (NO3)2、AgNO3
③Zn (NO3)2、Cu(NO3)2
④Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是(填标号),其理由是。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
| 实验步骤 |
现象 |
有关反应的化学方程式 |
| 取少量固体B, 滴加 |
有气泡产生 |
(3)下图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和;有铁生成的化学方程式为。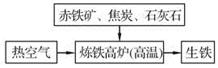
(4)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁。现有废硫酸49 t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少?