在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)  CO(g)+H2O(g),其平衡常数K与温度t的关系如下表:
CO(g)+H2O(g),其平衡常数K与温度t的关系如下表:
| T |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式: c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
在此温度下,若该容器中含有1molCO2、 1.2molH2、 0.75molCO、 1.5molH2O,这状态 (是或否)处于平衡状态?若不是,反应向哪个方向进行?
在一个固定容积的密闭容器中,保持一定温度,发生反应A(g)+B(g) 2C(g)已知加入1mol A和2molB,在达到平衡后生成了amolC,此时C在平衡混合物中的体积分数为M%.在相同实验条件下,
2C(g)已知加入1mol A和2molB,在达到平衡后生成了amolC,此时C在平衡混合物中的体积分数为M%.在相同实验条件下,
(1)若往相同容器中加入2molA 4molB,平衡后C的物质的量为__________mol.
(2)若往相同容器中加入0.5molC,若要求平衡后C的物质的量为0.5amol.平衡后C的体积分数仍为M%,则还应往容器中加入A _____________mol,B_______________mol.
(3)若往相同容器中加入2molA、6molB,若要求平衡后C的体积分数仍为M%,则应加入C___________mol,平衡后C的物质的量为___________mol.
如图甲乙丙三个烧杯依次分别盛放氢氧化钠溶液、硫酸铜溶液、硫酸钾溶液,电极均为石墨电极,通电一段时间,乙中c电极质量增加64克,据此回答问题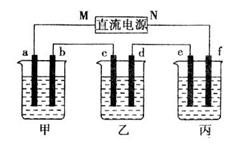
①电源的N端为 ___________极
②电极b上发生的电极反应为__________________________________
③电极b上生成的气体在标准状况下的体积______________________升
④电极e上生成的气体在标准状况下的体积_______________________升
将物质的量均为2. 00mol的物质X、Y混合,发生如下反应:2X+Y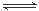 2W。在反应过程中W的物质的量分数随温度变化如图所示:
2W。在反应过程中W的物质的量分数随温度变化如图所示: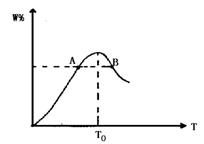
(1)T0对应的V正和V逆的关系是V正V逆(填“>”、“<”或“=”);
(2)此反应的正反应为热反应;
(3)A、B两点正反应速率的大小关系是AB(填“>”、“<”或“=”);
现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率_________,B的转化率_________。
(4)若升高温度,则平衡时B、C的浓度之比将_________。
(5)若加入催化剂,平衡时气体混合物的总物质的量_________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
一定温度下将3molA和1molB气体通入体积为2L的密闭恒容容器中,发生反应3A(g)+ B(g) xC(g)2min时反应平衡,剩余0.8molB,并测得C的浓度为0.4mol/L.
xC(g)2min时反应平衡,剩余0.8molB,并测得C的浓度为0.4mol/L.
回答问题
(1)从开始反应到达平衡,生成C的平均反应速率为________________
(2) x=________________
(3)若继续向原平衡混合物的容器中通入少量氦气,化学平衡___________(填字母)
A.向正反应方向移动
B. 向逆反应方向移动
C.不移动
(4)若向原平衡混合物的容器中再充入amolC,在原温度下达新的平衡,此时B的物质的量 n(B)=_______________mol