科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)写出CO燃烧的热化学方程式_____ ________;
(2)写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________;
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
①温度升高该反应的平衡常数 (增大、减小、不变)
②B过程用H2表示该反应的化学反应速率是 mol·L-1·min-1
(4)在直接以甲醇为燃料的电池中,电解质溶液为碱性,总反应为:CH3OH+3/2O2+2OH-==CO32-+3H2O,负极的反应式为 。
常温下,浓度均为0.1 mol·L-1的四种溶液:
①Na2CO3溶液②NaHCO3溶液③盐酸④氨 水
水
试回答下列问题:
(1)上述溶液中有水解反应发生的是 (填编号,下同),溶液中溶质存在电离平衡的是 ;
(2)比较①、②溶液,PH值较大的是 ;
(3)在溶液④中加入少量NH4Cl固体,此时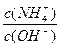 的值
的值
将 (填“变小”,“变大”或“不变”);
(4)用溶液③滴定V mL溶液④,其滴定曲线如下图所示: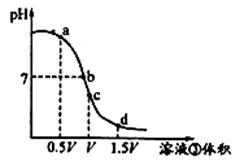
①试分析在滴定过程中,滴定曲线上a、b、c、d四点:
水的电离程度最大的是 点;
②取少量c点溶液于试管,再滴加0.1 mol/L NaOH溶液至中性。此时溶液中除H+、OH-外,其它离子浓度由大到小的顺序是 。
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 0.2
0.2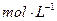 的醋酸溶液,用0.2
的醋酸溶液,用0.2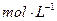 的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250 0.2
0.2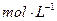 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、
醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、
。
(2)为标定某醋酸溶液的准确浓度,用0.2000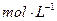 的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 |
1 |
2 |
3 |
4 |
| 消耗NaOH溶液的体积(mL) |
20.05 |
20.00 |
18.80 |
19.95 |
则该醋酸溶液的准确浓度为 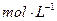 。(保留小数点后四位)
。(保留小数点后四位)
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,结果如下:
| 醋酸浓度 (mol·L–1) |
0.00l0 |
0.0100 |
0.0200 |
0.1000 |
| pH |
3.88 |
3.38 |
3.23 |
2.88 |
回答下列问题:
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是
。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度 。(填“增大”、“减小”或“不变”)
实验三 探究温度对醋酸电离程度的影响
(5)请你设计一个实验完成该探究,请简述你的实验方案
。
(12分)现有①0.2 mol/L NaOH溶液 ②0.2 mol/LHX溶液,两溶液等体积混合后,测得溶液中c(Na+)>c(X-)。则:
(1)①中由水电离出的c(OH-)②中由水电离出的c(H+)(填“>”、“<”或“=”)。
(2)上述混合液中共存在种粒子,且c(HX)c(X-)(填“>”、“<”或“=”,下同),c(HX)+c(X-)0.1 mol/L(忽略体积变化)。
(3)上述混合液显性(填“酸”、“碱”或“中”),其原因用离子方程式表示为。
已知KMnO4和H2C2O4在酸性溶液中发生反应:
KMnO4+H2C2O4+H2SO4—K2SO4+MnSO4+CO2↑+H2O(请配平)。
甲、乙两个实验小组欲探究影响化学反应速率的因素,设计实验方案如下:
(1)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小,实验装置如图所示。
实验时A溶液一次性放下,A,B的成分见下表:
| 序号 |
A溶液 |
B溶液 |
| ① |
2mL 0.1 mol·L-1 H2C2O4溶液 |
4mL 0.01 mol·L-1 KMnO4溶液 |
| ② |
2mL 0.2 mol·L-1 H2C2O4溶液 |
4mL 0.01 mol·L-1 KMnO4溶液 |
| ③ |
2mL 0.2 mol·L-1L H2C2O4溶液 |
4mL 0.01 mol·L-1 KMnO4溶液、少量催化剂 |
该实验探究的是对化学反应速率的影响。在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序是(用实验序号填空)。
(2)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速 率的大小。取两支试管各加入2
率的大小。取两支试管各加入2 0.1
0.1 H2C2O4溶液,另取两支试管各加入4
H2C2O4溶液,另取两支试管各加入4 0.1
0.1 KMnO4溶液。将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验试图探究对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是。
KMnO4溶液。将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验试图探究对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是。
A、B两种烃,其相关信息如下,请根据信息回答相关问题。
| A |
①完全燃烧的产物中n(CO2):n(H2O)=2:1 ②28<M(A)<60 ③不能使溴的四氯化碳溶液褪色 ④一氯代物只有一种结构 ⑤碳碳之间都是单键 |
B |
①饱和链烃,通常情况下是气态 ②有同分异构体 ③二溴代物有三种 |
(1)烃A的最简式为____________
(2)烃A的键线式为____________
(3)烃B的分子式为____________
(4)烃B的同分异构体的结构简式为_________________________