下面四个实验都是教材中的化学实验,请回忆并解决有关问题 (1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”) 。
(1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”) 。
(2)实验B是硫在氧气中燃烧实验,瓶中预先加水的目的是: 。小郑同学对该实验进行药品改进,把水替换为滴有酚酞试液的 溶液,实验时既能更好达到目的,又提高实验现象的趣味性。
(3)实验C是探究酸的化学性质实验,用点滴板代替试管完成实验的好处是 。
(4)实验D是蒸馏水的制取,蒸馏过程水的流向是 (填“下入上出”或“上入下出”);高温水蒸气的冷却,从微观角度看是水分子的 减小了。
(5)二氧化氮是一种密度大于空气易溶于水的有毒红棕色气体,用铜片与浓硝酸(HNO3)共微热就可以制得,同时生成硝酸铜和水。现请你回顾实验室制取气体的一般思路和方法,解决下列问题:
①、补全实验室制取NO2的化学方程式:
Cu + 4HNO3(浓)△ Cu(NO3)2 +2 NO2↑+ □
②、反应原理决定实验装置的设计。根据①的方程式,要制取一瓶NO2,至少要选择上面实验装置A、B、C、D中的铁架台、 、 烧瓶等仪器用于组装实验装 置,收集方法可采用 ,并进行必要的尾气处理。整套实验装置设计组装完毕后必须检查 。
③、请你预测制取NO2时的实验现象:(至少答两点)
Ⅰ: ;Ⅱ: 。
④、反应后所得溶液通过 (填操作名称)可以获得硝酸铜晶体。
小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
[知识回放]
金属活动性顺序:K Ca Na Mg Al ZnSn Pb(H)Hg Ag Pt Au,请你在横线上填写对应金属的元素符号。
[作出猜想]
猜想1.Cr>Fe>Cu;猜想2.Fe>Cu>Cr;猜想3.你的猜想是。
[查阅资料]
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
[设计实验]
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸
| 实验 |
试管1 |
试管2 |
试管3 |
| 实验 操作 |
 |
 |
 |
| 实验 现象 |
铁片表面产生气泡较慢,溶液变为浅绿色 |
铬片表面产生气泡较快,溶液变成为蓝色 |
[结论与解释]
(1)小聪得到的结论是猜想正确。
(2)实验前用砂纸打磨金属片的目的是。
[知识运用]
将铬片投入FeSO4溶液中,反应(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式。
某无土栽培营养液的配方中可能含有氯化钾、硫酸铵、碳酸氢氨中的一种或几种物质,为确定配方的成分,化学兴趣小组的同学开展了以下探究活动:
(1)【实验探究一】取少量固体样品在研体中与熟石灰混合研磨,有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变色,写出可能发生该反应的一个化学方程式。
(2)【实验探究二】另取少量固体样品溶于水得到溶液A,按下图所示进行实验,现象如图所述(设发生的反应都恰好完全进行).请你回答下列问题: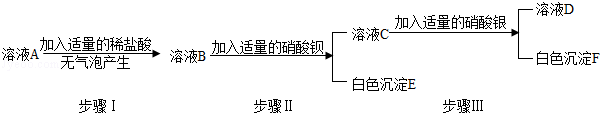
①白色沉淀E是。
②小明认为由实验探究二可以确定该化肥中一定含有氯化钾和硫酸铵,一定没有碳酸氢铵。小强认为这个结论不正确,他的理由。为了使小明的结论正确,小强对上述实验进行了改动,他的做法是。
在实验课中,各小组作了如下实验:
| 实验编号 |
1 |
2 |
3 |
4 |
| 实验操作 |
 |
 |
 |
 |
实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁…,应该可以从中提炼出铁和铜。经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶质相同。
则固体C是,操作③的名称是,实验中所加的过量金属粉末是。
对比学习有利于发现事物的共性与个性。为探究酸的性质,同学们进行了如下实验。
| 实验内容 |
实验现象 |
分析与结论 |
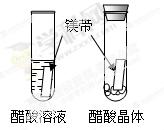 |
醋酸晶体试管内 (1),醋酸溶液试管中镁带表面冒气泡。 |
酸的很多反应通常在水溶液中才能完成。 |
用玻璃棒蘸硫酸在白纸上写字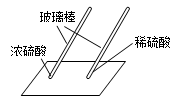 |
(2)(填“浓”或“稀”)硫酸使白纸炭化。 |
即使是同种酸,由于(3) 不同,它们的性质不完全相同。 |
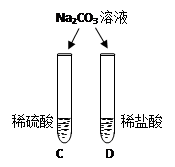 |
两试管中均产生(4) |
不同的酸具有相似的性质,这是因为酸的组成中都含有(5)(填元素符号)。 |
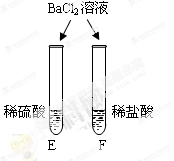 |
E试管中产生(6) , F试管中无明显现象。 |
不同的酸根会导致酸的“个性”差异。因此,可用氯化钡溶液鉴别盐酸和硫酸。 |
清洗试管时,小乔同学将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。请分析上述现象并回答:
Ⅰ.废液缸中产生气体的化学方程式为(7) 。
Ⅱ. 废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有(8) (填化学式)。
金属材料在国防建设中起着量要的作用,图1为歼﹣15飞机在辽宁舰上起飞
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是、。
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的共同作用的结果,工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为。
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是。
②实验二中,若出现现象,可证明铁的活动性强于铜,该反应的化学方程式为。
(4)辽宁舰的建造耗费了大量的钢材.某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称量赤铁矿样品的质量为wg)。
①装置A中生成铁的化学方程式为,装置B中发生反应的化学方程式为。
②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是。