在容积为2 L的密闭容器中,有反应:mA(g)+nB(g) pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了a mol·L-1, B的平均反应速率vB=a/15 mol·(L·min)-1,C增加了2a/3 mol·L-1,这时,若增加系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了a mol·L-1, B的平均反应速率vB=a/15 mol·(L·min)-1,C增加了2a/3 mol·L-1,这时,若增加系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
| A.3∶1∶2∶2 | B.1∶3∶2∶2 | C.1∶3∶2∶1 | D.1∶1∶1∶1 |
目前科学家普遍认为,质子和中子都是由被称为u夸克和d夸克的两类夸克构成,u夸克带电量为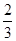 e,d夸克带电量为-
e,d夸克带电量为-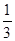 e,e为基元电荷,下列论断中可能正确的是( )
e,e为基元电荷,下列论断中可能正确的是( )
| A.质子是由1个u夸克和1个d夸克构成,中子是由1个u夸克和2个d夸克构成的 |
| B.质子是由2个u夸克和1个d夸克构成的,中子是由1个u夸克和2个d夸克构成的 |
| C.质子是由1个u夸克和2个d夸克构成的,中子是由2个u夸克和1个d夸克构成的 |
| D.质子是由2个u夸克和1个d夸克构成的,中子是由1个u夸克和1个d夸克构成的 |
将等物质的量浓度、等体积的硫酸与烧碱溶液混合后,滴入紫色石蕊试液,溶液呈( )
| A.紫色 | B.红色 | C.蓝色 | D.无色 |
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述中正确的是( )
| A.1.01×105 Pa、25 ℃时,2.24 L Cl2中含有的原子数为0.2×6.02×1023 |
| B.0.1 L 3 mol·L-1 NH4NO3溶液中含有的N原子数目为0.3×6.02×1023 |
| C.5.6 g铁粉与足量CuSO4溶液反应生成的铜原子数为1×6.02×1023 |
| D.46 g NO2和N2O4的混合物中含有的原子数为3×6.02×1023 |
对于某些离子的检验及其结论一定正确的是( )
| A.加入稀盐酸产生无色无味气体,将气体通入石灰水中,变浑浊,一定有CO32- |
| B.加入BaCl2溶液产生白色沉淀,再加上稀盐酸沉淀不消失,一定有SO42- |
| C.加入足量稀盐酸无沉淀,再加BaCl2溶液有白色沉淀,一定有SO42- |
| D.加入Na2CO3溶液产生白色沉淀,再加稀盐酸白色沉淀消失,一定有Ba2+ |
下列反应类型的判断,不正确的是( )
A.CO2+H2O H2CO3化合反应 H2CO3化合反应 |
B.Cu(OH)2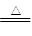 CuO+H2O 分解反应 CuO+H2O 分解反应 |
C.MnO2+2CO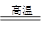 Mn+2CO2置换反应 Mn+2CO2置换反应 |
| D.NaCl+AgNO3=AgCl↓+NaNO3复分解反应 |