下列叙述中,正确的是:
| A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 |
| B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C.晶体中只要有阳离子就会有阴离子 |
| D.电子数相同的阳离子和阴离子一定不具有相同的质子数 |
下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热 kJ/mol,则H2SO4和Ca(OH)2反应的中热 kJ/mol,则H2SO4和Ca(OH)2反应的中热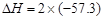 kJ/mol kJ/mol |
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的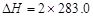 kJ/mol kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
“熵”可看作是“混乱度”,它的符号是“S”。下列变化中,△S<0(“混乱度”减小)的是
| A.3Fe(s)+4H2O(g) =Fe3O4(s)+4H2(g) |
| B.2NO2(g) =N2O4(l) |
| C.2IBr(l) =I2(s)+Br2(g) |
| D.(NH4)2CO3(s) =2NH3(g)+CO2(g)+2H2O(g) |
100 mL 6 mol/L H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速度,但又不影响生成氢气的总量,不可向反应物中加入适量的
| A.碳酸钠(固体) | B.水 |
| C.硫酸钾溶液 | D.CH3COONa(固体) |
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中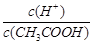 值增大,可以采取的措施是
值增大,可以采取的措施是
| A.加少量烧碱溶液 | B.降低温度 |
| C.加少量冰醋酸 | D.加水 |
在同温同压下,合成氨反应N2+3H2=2NH3进行到某时刻达到平衡.起始时N2和H2共120体积,平衡时总体积为70体积,则原混合气体中N2和H2的体积比可能为:
| A.1:3 | B.9:15 | C.5:19 | D.1:1 |