实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0)。试回答下列问题:
(1)写出反应过程中的离子反应方程式:
OC段 ,
DE段 ,
EF段___________________________________ __________。
(2)硝酸溶液的物质的量浓度为 mol·L-1
(3)B的值为_________mol,C的值为 mL。
[化学——选修3:物质结构与性质]1967年舒尔滋提出金属互化物的概念,其定义为固相金属间化合物拥有两种或两种以上的金属元素,如 等。回答下列问题:
等。回答下列问题:
(1)某种金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于 (填“晶体”或“非晶体”)。
(2)基态铜原子有 个未成对电子,二价铜离子的电子排布式为 ,在CuS04溶液中滴入过量氨水,形成配合物的颜色为 。
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2,1 mol(SCN)2分子中含有共价键的数目为 ;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N="C=S" )的沸点,其原因是 。
(4)ZnS的晶胞结构如图1所示,在ZnS晶胞中,S2-的配位数为 。
(5)铜与金形成的金属互化物结构如图2,其晶胞边长为a nm,该金属互化物的密度为 (用含“a、NA的代数式表示)g· 。
。
雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ的目的是 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。
①若是0.1molNaOH反应后的溶液,测得溶液的pH=4时,溶液中各离子浓度由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)写出装置Ⅱ中,酸性条件下反应的离子方程式 , 。
(4)装置Ⅲ中阴极反应方程式为 ;阳极使Ce4+再生,其原理如图所示。生成Ce4+从电解槽的 (填字母序号)口流出。
(5)若进入装置Ⅳ的溶液中的NO2-完全转化为NH4NO3, 反应中氧化剂与还原剂的物质的量之比为。
[化学——选修5:有机化学基础]高分子材料PET聚酯树脂和PMMA的合成路线如下:
已知:
Ⅰ.RCOOR′+ R′′18OH  RCO18O R′′+ R′OH(R、R′、R′′代表烃基)
RCO18O R′′+ R′OH(R、R′、R′′代表烃基)
Ⅱ.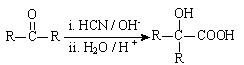 (R、R′代表烃基)
(R、R′代表烃基)
(1)①的反应类型是________。
(2)②的化学方程式为________。
(3)PMMA单体的官能团名称是________、________。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为________。
(5)G的结构简式为________。
(6)下列说法正确的是________(填字母序号)。
a.⑦为酯化反应
b.B和D互为同系物
c.D的沸点比同碳原子数的烷烃高
d.1 mol 与足量NaOH溶液反应时,最多消耗4 mol NaOH
(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是________。
(8)写出由PET单体制备PET聚酯(化学式为C10nH8nO4n 或C10n+2H8n+6O4n+2)并生成B的化学方程式 。
[化学——选修3:物质结构与性质]已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态。
请填写下列空白。
(1)E元素基态原子的核外电子排布式为_________________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为_____________(填元素符号),其原因为_____________________。
(3)B2A4是重要的基本石油化工原料。B2A4分子中B原子轨道的杂化类型为__________;
1 mol B2A4分子中含__________molσ键。
(4)已知D、E能形成晶胞如图所示的两种化合物,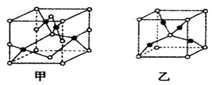
化合物的化学式,甲为_________,乙为_________;高温时,甲易转化为乙的原因为_______________。
Ⅰ.2011年11月28日至12月9日,联合国气候变化框架公约第17次缔约方会议在南非德班召开,随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25 mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O (g)的浓度随时间变化如图所示: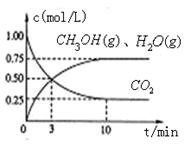
① 写出该工业方法制取甲醇的化学反应方程式 。
② 从反应开始到平衡,氢气的平均反应速率v (H2)= 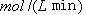 。
。
③ 该条件下CO2的转化率为 。当温度降低时CO2的转化率变大,则该反应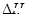 0(填“>”“<”或“=”)。
0(填“>”“<”或“=”)。
④ 下列措施中能使n(CH3OH)/n(CO2)增大的是 。
| A.升高温度 | B.充入氮气 |
| C.将水蒸气从体系中分离 | D.用更有效的催化剂 |
(2)选用合适的合金作为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极的电极方程式为 。
Ⅱ.研究NO2 、SO2 、CO等大气污染气体的处理具有重要意义。其中氮元素有着多变价态和种类多的化合物,它们在工农业生产、生活中发挥着重要的作用。完成下列问题:
(1)已知:2SO2(g) + O2(g) 2SO3(g) ΔH=" —196.6" kJ·mol―1
2SO3(g) ΔH=" —196.6" kJ·mol―1
2NO(g) + O2(g) 2NO2(g)ΔH=" —113.0" kJ·mol―1
2NO2(g)ΔH=" —113.0" kJ·mol―1
则反应NO2(g) + SO2(g) SO3(g) + NO(g) 的ΔH= 。
SO3(g) + NO(g) 的ΔH= 。
(2)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,
①下列能说明反应达到平衡状态的是 (填序号) 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.相同时间内,每消耗1 molNO2的同时消耗1 mol SO3
②当测得上述反应平衡时NO2与SO2体积比为1: 6,则平衡常数K= 。