一定的温度下向2L密闭容器中通入2molSO2和2molO2,发生反
应: 2SO2+O2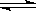 2SO3.5min后达到平衡,测得容器中有SO31.6mol.
2SO3.5min后达到平衡,测得容器中有SO31.6mol.
回答下列问题:
(1) 反应5min内,v(O2)=_________mol.L-1.min-1.
(2) 化学反应达到平衡时,SO2消耗的浓度占起始浓度的百分比为__________;此时,容器中c(O2)=_______,压强是起始时的_______倍.
(3) 判断该反应达到平衡的标志是_______________;
| A.v消耗(SO2)=v生成(SO3) | B.混合气体的平均相对分子质量不再改变 |
| C.混合气体的密度不再改变 | D.容器中气体的总物质的量不再变化 |
四氯化钛是无色液体,沸点为136℃。它极易水解,遇空气中水蒸气即产生“白烟”(TiCl4+H2O TiOCl2+2HCl↑)。在650~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。下图是实验室制备TiCl4的部分装置。
TiOCl2+2HCl↑)。在650~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。下图是实验室制备TiCl4的部分装置。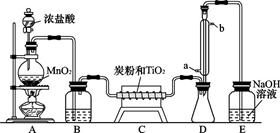
请回答:
(1)B装置中试剂为,其作用是(每空l分)。
(2)C装置中的反应方程式为。
(3)D装置中冷凝水的方向为进出,该装置的作用为。
(4)评价此装置的缺陷和不妥之处(每空2分):
| 编号 |
装置缺陷和不妥之处 |
| ① |
|
| ② |
|
| ③ |
回答下列各小题:
(1)已知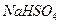 在水中的电离方程式为
在水中的电离方程式为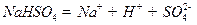 。在
。在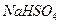 溶液
溶液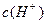 __________
__________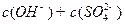 (填“>”“=”或“<”,1分)。
(填“>”“=”或“<”,1分)。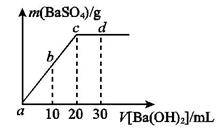
(2)常温下,向1.0mol/L的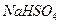 溶液中逐滴加入等物质的量浓度的
溶液中逐滴加入等物质的量浓度的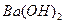 溶液,生产沉淀的量与加入氢氧化钡溶液的体积关系如图所示。a、b、c、d分别表示实验时不同阶段的溶液。其中b点表示溶液呈_________(填“酸性”“中性”或“碱性”,1分),c点所示的离子方程式为______________________________________________________。
溶液,生产沉淀的量与加入氢氧化钡溶液的体积关系如图所示。a、b、c、d分别表示实验时不同阶段的溶液。其中b点表示溶液呈_________(填“酸性”“中性”或“碱性”,1分),c点所示的离子方程式为______________________________________________________。
(3)在T℃时,将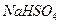 晶体加入到pH=6的蒸馏水中,保持温度不变,测得溶液的pH为2。T℃将__________25℃(填“高于”或“低于”,1分),K
晶体加入到pH=6的蒸馏水中,保持温度不变,测得溶液的pH为2。T℃将__________25℃(填“高于”或“低于”,1分),K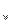 为__________,在该溶液中由水电离出的
为__________,在该溶液中由水电离出的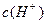 为__________mol·L-1。T℃时,将pH=11的NaOH溶液V1L与pH=1的
为__________mol·L-1。T℃时,将pH=11的NaOH溶液V1L与pH=1的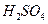 溶液V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1: V2 =____________,此溶液中各种离子的浓度由大到小的排列顺序为________________________________________________。
溶液V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1: V2 =____________,此溶液中各种离子的浓度由大到小的排列顺序为________________________________________________。
(4)0.1 mol·L-1pH为4的NaHB溶液中①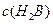 、②
、②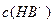 、③
、③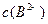 由大到小的顺序为_______________。
由大到小的顺序为_______________。
(5)在0.1 mol·L-1的①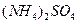 溶液、②
溶液、②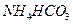 溶液、③
溶液、③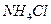 溶液中,
溶液中,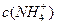 由大到小的排列顺序为_______________________。
由大到小的排列顺序为_______________________。
某有机物A在一定条件下的转化关系如图所示,其中两分子E生成环状化合物F,D的结构简式为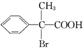 。
。
已知 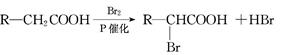
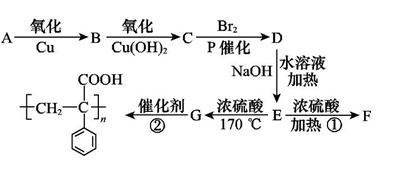
回答下列问题:
(1)写出反应类型:① ,② (每空1分)。
(2)写出有机物C、F的结构简式: 、 (每空2分)。
(3)写出下列化学方程式:A→B: ,E→G: (每空2分)。
(4)C的同分异构体有多种,其中属于苯的二取代物,且既能有银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有6种,请写出其中任意一种的结构简式: 。
有A、B、C、D、E、F、G七种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径B>C;
②D、E、G是非金属元素,它们都可以跟氢化合生成气态氢化物HD、HE和HG,在室温时,G的单质与氢气暗处混合就爆炸,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体。
(1)A的名称是,B位于周期表中第周期族,C的原子结构示意图是
(每空l分)。
(2)E的单质颜色是。
(3)A元素与D元素形成化合物的电子式是。
(4)G的单质与水反应的化学方程式是。
(5)F的元素符号是。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的化学式是,酸性最强的化学式是,气态氢化物最稳定的化学式是(每空l分)。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
。
(15分)
阅读分析材料,据此完成下列要求。
某芳香族化合物A的化学式微C8H8Cl2,它有如下转换关系:
 |
(1)X为,反应I的反应类型为,N分子中含氧官能团的名称为。
(2)反应Ⅱ的化学方程式为:。
(3)苯环上的一溴代物只有一种,与A互为同分异构体的物质有种,写出其中一种的结构简式。
(4)检验A分子中的卤素原子,简述实验方案。