四氯化钛是无色液体,沸点为136℃。它极易水解,遇空气中水蒸气即产生“白烟”(TiCl4+H2O TiOCl2+2HCl↑)。在650~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。下图是实验室制备TiCl4的部分装置。
TiOCl2+2HCl↑)。在650~850℃下,将氯气通过二氧化钛和炭粉的混合物可得到四氯化钛和一种有毒气体。下图是实验室制备TiCl4的部分装置。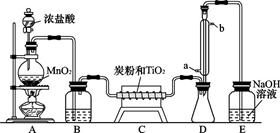
请回答:
(1)B装置中试剂为 ,其作用是 (每空l分)。
(2)C装置中的反应方程式为 。
(3)D装置中冷凝水的方向为 进 出,该装置的作用为 。
(4)评价此装置的缺陷和不妥之处(每空2分):
| 编号 |
装置缺陷和不妥之处 |
| ① |
|
| ② |
|
| ③ |
|
一定条件下,在体积为3 L的密闭容器中有反应:
CO(g)+2H2(g) 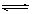 CH3OH(g) (催化剂为Cu2O/ZnO),根据题意完成下列各题:
CH3OH(g) (催化剂为Cu2O/ZnO),根据题意完成下列各题: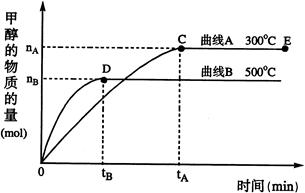
(1)反应达到平衡时,平衡常数表达式K=,升高温度,K值 (填“增大”、“减小”或“不变”);
(2)在500℃,从反应开始到平衡,H2的平均反应速率v(H2)=(用nB、tB表示);
(3)下列描述中能说明上述反应已达平衡的是;
a.v(CO)=2v(H2)
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(4)开始向密闭容器中充入0.10 molCO和0.20 molH2,一段时间后达到平衡,测得容器中CH3OH物质的量为0.08 mol;若再通入0.10 molCO和0.20 molH2,则平衡移动 (填“正向”、“逆向”或“不”);若平衡移动,再次达到平衡后,mol<n(CH3OH)<mol。
日常生活中的塑料包括很多种,其中PET(聚对苯二甲酸乙二醇酯)塑料被广泛用于生产包装瓶、电器元件、汽车配件等;PS塑料被广泛应用于光学工业中,PET塑料、PS塑料可按下图所示合成。
(1)C能与含氧酸发生酯化反应,则C的分子式为,其所含的官能团的名称为。
(2)X、Y互为同分异构体,分子式为C8H10,则X的结构简式为,
其核磁共振氢谱有种峰。
(3)D分子中含有一个甲基,则D→E的化学方程式为,
E与CH2=CH—CH=CH2在一定条件下1︰1发生反应生成除苯环外无支链的高聚物的化学方程式为。
(4)Z是B的同分异构体,其具有如下性质:①遇FeCl3溶液显紫色;②能与NaHCO3溶液反应放出CO2;③苯环上的一氯代物只有三种;④苯环上只有2个取代基相邻。则Z的结构最多有种,写出其中一种的结构简式。
下表是A、B、X、Y、Z五种有机物的有关信息:
| A |
 B B |
X |
Y |
Z |
|||
| ①能使溴的四氯化碳溶液褪色; ②比例模型为:
|
①由C、H两种元素组成; ②球棍模型为:  |
①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与Z反应生成相对分子质量为100的酯。 |
①相对分子质量比X少2; ②能由X氧化而成; |
①由C、H、O三种元素组成; ②球棍模型为:  |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称叫做 ,写出在一定条件下,A生成高分子化合物的化学反应方程式__ _____。
(2) A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=__________时,这类有机物开始出现同分异构体。
(3) B具有下列性质中的哪些? (填号):
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色⑥任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: 。
(4)X与Z反应能生成相对分子质量为100的酯,该反应类型为 ;其化学反应方程式为: 。
(5) 写出由X氧化生成Y的化学反应方程式: 。
为了测定某饱和卤代烃的分子中卤原子的种类和数目,可按下列步骤进行实验: 回答下列问题:
回答下列问题:
(1)准确量取11.40 mL液体所用仪器是________;
(2)加入过量硝酸的作用是___________________________________________;
(3)加入AgNO3溶液时产生的沉淀为浅黄色,则此卤代烃中的卤原子是________;
(4)已知此卤代烃液体的密度是1.65 g/mL,其蒸气对甲烷的相对密度是11.75,则此卤代烃每个分子中卤原子的数目为_______个;此卤代烃的结构简式为:_。
下表是元素周期表的一部分,表中所列的字母分别代表某一种化学元素。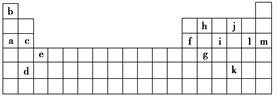
(1)上述第三周期元素中第一电离能(I1)最大的是________(用字母表示,下同),c和f的I1大小关系是________大于________。
(2)上述元素中,原子中未成对电子数最多的是________,写出该元素的电子排布式:________________。
(3)根据下表所提供的电离能数据,回答下列问题。
| 锂 |
X |
Y |
|
| I1 |
519 |
502 |
580 |
| I2 |
7296 |
4570 |
1820 |
| I3 |
11799 |
6920 |
2750 |
| I4 |
9550 |
11600 |
①表中X可能为以上13种元素中的________元素。用元素符号表示X和j形成的化合物的化学式________。
②Y是周期表中的________族的元素。