(9分)将铂丝插入稀硫酸溶液作电极,然后向两个电极上分别通入甲烷和氧气,可以形成原电池,由于发生的反应类似于甲烷的燃烧,所以称作燃料电池。根据两极上反应的实质判断,通入甲烷的一极为电池的__ _极,通入氧气的一极的电极反应式为_______________,该燃料电池放电一段时间后溶液的浓度将__________(选填“增大”,“减小”或“不变”)
(1)通常用小苏打的悬浊液除去CO2中的HCl,反应的离子方程式为:,
不能用NaOH溶液的原因是,也不能用Na2CO3的原因是(均用离子方程式表示原因)
(2).把下列离子方程式改写成化学方程式:
CO32- + 2H+ = CO2↑ + H2O
Ag+ + Cl-= AgCl↓
(1)下列各组中的两种有机物,可能是相同的物质、同系物或同分异构体等,请判断它们之间的关系
①2-甲基丁烷和丁烷。
②1-已烯和环已烷。
(2)支链只有一个乙基且式量最小的烷烃的结构简式。
(3)写出乙醛溶液与足量的银氨溶液共热的化学方程式:;
(4)写出1,3-丁二烯与溴单质发生1,4-加成的反应方程式
(5)写出由乙醇一步制溴乙烷的化学方程式
部分难溶物的颜色和常温下的Ksp如下表所示:
| Cu(OH)2 |
CuOH |
CuCl |
Cu2O |
|
| 颜色 |
蓝色 |
黄色 |
白色 |
砖红色 |
| Ksp(25 ℃) |
1.6×10-19 |
1.0×10-14 |
1.2×10-6 |
— |

某研究性学习小组对电解食盐水进行了如下探究:
实验Ⅰ 装置如图所示,接通电源后,发现a、b电极上均有气泡产生。
(1)电解过程中的总离子反应方程式为_________________________________________。
(2)为了确定电源的正、负极,下列操作一定行之有效的是 。
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ 把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示。
观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5 min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10 min后,最靠近a极的白色沉淀开始变成红色;
④12 min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色。
(3) a极发生的电极反应方程式为________________________________________________________。
(4) 电解5 min后,b极发生的电极反应方程式为___________________________________________。
(5)12 min后,b极附近出现的橙黄色沉淀的成分是 ,原因是___________________________________________________________________________________。
(10分)电解原理和原电池原理是电化学的两个重要内容。某兴趣小组做如下探究实验:
Ⅰ.(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)_______________________________设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________mol电子。
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为________________________,这是由于NH4Cl溶液显________(填“酸性”“碱性”或“中性”),用离子方程式表示溶液显此性的原因____________________________________________。
(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则乙装置中石墨(1)为________极(填正、负、阴、阳),乙装置中与铜线相连石墨电极上发生的反应式为_________________________________。
Ⅱ.如右图所示装置,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL。
请完成下列问题:
①第②极上生成的物质为________mol。
②写出第①极上发生反应的电极反应式_________________________。
③设A池中原混合液的体积为200 mL,则通电前A池原混合液中Cu2+的浓度为________ mol/L。
(8分)草酸(H2C2O4)是二元弱酸,25℃时,H2C2O4:K1=5.4×10-2,K2=5.4×10-5;H2CO3:K1=4.5×10-7,K2=4.7×10-11。
(1)KHC2O4溶液呈__________性(填“酸”、“中”或“碱”)。
(2)下列化学方程式可能正确的是。
A.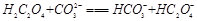 |
B.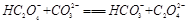 |
C.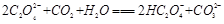 |
D.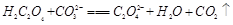 |
(3)常温下,向10 mL 0.01 mol·L-1H2C2O4溶液中滴加0.01 mol·L-1的KOH溶液V mL,回答下列问题:
①当V<10时,反应的离子方程式为______________________________________________。
②若溶液中离子浓度有如下关系:c(K+)=2c(C2O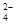 )+c(HC2O
)+c(HC2O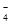 ),则pH______7(填“>”“<”或“=”),V________10(填“>”“<”或“=”)。
),则pH______7(填“>”“<”或“=”),V________10(填“>”“<”或“=”)。
③当溶液中离子浓度有如下关系:c(K+)=c(C2O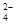 )+c(HC2O
)+c(HC2O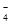 )+c(H2C2O4),则溶液中溶质为____________,V________10(填“>”、“<”或“=”)。
)+c(H2C2O4),则溶液中溶质为____________,V________10(填“>”、“<”或“=”)。
④当V=20时,溶液中HC2O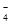 、C2O
、C2O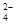 、H2C2O4、OH-的物质的量浓度从大到小的顺序为____________________________________________________________________________________。
、H2C2O4、OH-的物质的量浓度从大到小的顺序为____________________________________________________________________________________。