下列有机物:
①HOCH2CH2OH ②HOCH2CH(OH)CH2OH
③(CH3)3CCH2OH ④(CH3)3COH ⑤C(CH2OH)4
⑥CH3CH2-O-CH2CH3 ⑦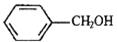
(1)不能发生消去反应的醇是: 。
(2)不能发生催化氧化(去氢氧化)的醇是: 。.
(3)互为同系物的是: 。
(4)互为同分异构体的是: 。
我国是氧化铝生产大国,工业上每生产1 t氧化铝将排出1~2 t赤泥,赤泥大量堆积会对环境造成严重污染。赤泥中主要成分及含量:CaO约占46%、SiO2约占22%、Al2O3约占7%、Fe2O3约占11%、TiO2约占5%及少量其他物质。
⑴一种利用废弃赤泥的方法是将赤泥配成一定的液固比,作为一种吸收剂,吸收热电厂排放的含SO2的烟气,写出吸收SO2时可能发生的化学反应方程式 ▲。
⑵为综合利用赤泥中的各种成分,某科研小组设计了如下工艺流程:
 |
已知:TiO2不溶于稀盐酸、稀硫酸,能溶于浓硫酸生成TiOSO4(硫酸氧钛,易水解)。
①氧化物D的化学式是 ▲,原料A最好是下列物质中的 ▲。
| A.氨水 | B.氢氧化钠 | C.生石灰 | D.双氧水 |
②写出上述工艺中投入氢氧化钠时反应的离子方程式 ▲。
③写出上述工艺中稀释时发生水解反应的化学方程式 ▲。
以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表。
| 难溶物 |
Ksp |
| Ca3(AsO4)2 |
6.8× 10-19 10-19 |
| AlAsO4 |
1.6×1 0-16 0-16 |
| FeAsO4 |
5.7×10-21 |
| 污染物 |
H2SO4 |
As |
| 浓度 |
28.42 g/L |
1.6 g·L-1 |
| 排放标准 |
pH 6~9 |
0.5 mg·L-1 |
表1.几种砷酸盐的Ksp表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
⑴该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)= ▲mol·L-1。
⑵写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]= ▲,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,c(AsO43-)的最大是 ▲mol·L-1。
⑶工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 ▲。
⑷在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ▲;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为 ▲。
有机物W~H有如下的转化关系。已知W、B为芳香族化合物,X为卤素原子,W、A、B均能与NaHCO3溶液反应,A分子中有2个甲基,H分子中含有醛基且苯环请回答下列有关问题:
请回答下列有关问题:
(1)反应①、②分别属于反应、反应(填有机反应类型),
A、B中均含有的含氧官能团的名称是。
(2)F的化学式 ,B的结构简式。
,B的结构简式。
(3)反应②的化学方程式是。
(4)若
反应④的化学方程式是。
(5)H有多种同分异构体,写出任意一种同时满足(i)遇FeCl3显紫色(ii)苯环上—取代物有两种(iii)除苯环外无其它环状结构3个条件的H的同分异构体结构简式。
“温室效应”是哥奉哈根 世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
世界气候变化大会研究的环境问题之一。CO2气体在大气层中具有吸热和隔热的功能,是主要的温室气体。
(1)下列措施中,有利于降低大气中CO2浓度的是(填字母编号)。
a.采用节能技术,减少化石燃料的用量
b.鼓励乘坐公交车出行,倡导“低碳”生活
c.利崩太阳能、风能等新型能源替代化石燃料·
(2)CH4是另一种主要的温室气体,l克甲烷完全燃烧生成液态水和二氧化碳,放出55.64 kJ的热量,甲烷的燃烧热是。
(3)酸阿的形成主要是由废气中的SOx和NOx造成的。通过SO2和Br2、H2O的定量反应在电解池中产生的电流变化,可以准确测定空气中SO2的含量。该反应的化学方程式为,反应中氧化产物和还原产物的物质的量之比为。
(4)某硫酸工厂以黄铁矿为原料生产硫酸。
第一阶段燃烧黄铁矿的化学方程式为;
第二阶段的反应原理是2SO2(g)+O2(g) 2SO3(g),其生产设备的名称为;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为
2SO3(g),其生产设备的名称为;在生产过程中某一时刻取样分析:SO2、O2、SO3的浓度分别为
2mol·L-1、2mol·L-1、3mol·L-1,当反应达到平衡时,可能存在的数据是(填字母编号)
a. SO2为5mol·L-1,O2为3.5mol·L-1
b. SO2为3mol·L-1
c.SO2、SO3均为2.5mol·L-1
d.SO3为5mol·L-1
现有X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素。有关信息如下表:
| 原子或分子相关信息 |
单质及其化合物相关信息 |
|
| X |
ZX4分子空间结构为正四面体 |
X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y |
Y原子的最外层电子数等于电 |
Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料(人造刚玉) |
| Z |
Z原子的最外层电子数是次外层电子数的 |
Z是无机非金属材料的主角,其单质为原子晶体,是一种优良的半导体材料 |
| W |
W原子的最外层电予数小于4 |
W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1)W位于周期表第四周期第族,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为。
(2)Z最简单的氧化物分子是分了(填“极性”或“非极性”):工业上用Z的氧化物制备其单质的化学反应方程式为。
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它最常用来制造晶体篱,最新研究表明:有机锗具有明显的抗肿瘤活性,锗元素的最高价氧化物的化学式为。
(3)实验室制取X单质的离子方程式为;X的气态氧化物的水溶液与Y的氧化物反应的离子方程式为。
(4)在50mL lmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能为mL或mL。