下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。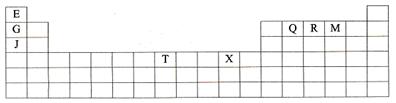
(1)T3+的核外电子排布式是:
(2)Q、R、M的第一电离能由大到小的顺序是 (用元素符号表示)
(3)根据下列说法填空:
①G单质的熔点高于J单质,是因为
②将J2M2溶于水,要破坏 (离子键、极性共价键、非极性共价键)
③RE3沸点高于QE4,是因为
④一个Q2E4分子中E的 轨道与Q的 轨道形成σ键。
(4)G与R单质直接化合生成一种离子化合物G3R。该晶体具有类似石墨的层状结构。每层中,G原子构成平面六边形,每个六边形的中心有一个R原子。层与层之间还夹杂一定数量的原子。请问这些夹杂的原子应该是 (填G或R的元素符号)
已知锌与稀硫酸反应为放热反应,某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气,实验记录如下:
| 经过时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
30 |
120 |
280 |
350 |
370 |
①反应速率最大的(即0~1 min、1~2 min、2~3 min、3~4 min、4~5 min)时间段为 ,原是 。
②反应速率最小的时间段为 ,原因是。
以甲醇、空气和氢氧化钾溶液为原料,金属铂为电极可构成普通的燃料电池。该电池的负极上的电极反应式为____________
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t时到达平衡,依图所示: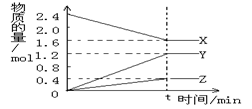
①该反应的化学方程式是 。
②反应起始至t,Y的平均反应速率是。
现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。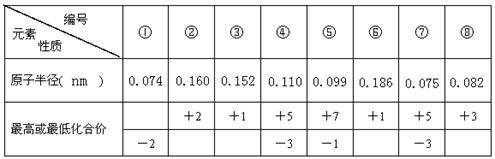
回答下列问题:
(1)①在元素周期表中的位置是(周期、族);
(2)比较④和⑦的氢化物的稳定性(用化学式表示)。
下表是元素周期表的一部分。根据表中的10种元素,用元素符号或化学式填空:
| 族 期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
① |
|||||||
| 2 |
② |
③ |
||||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||
| 4 |
⑨ |
⑩ |
(1)在①~⑩元素中,金属性最强的金属元素是________。
(2) 在①~⑩元素中,________(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的化学方程式是_______________________。
(3)在①~⑩元素中,形成的最高价氧化物的水化物的酸性最强的酸的分子式是________。
(4)④、⑥、⑦、⑨所形成的单核离子中,半径最大的离子是________。
(5)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。a.MnO2 b.FeCl3c.Na2SO3 d.KMnO4
(6)用电子式表示元素⑦与元素⑨形成的化合物的形成过程:。
用电子式表示元素⑥与元素①形成的化合物的形成过程:。
(7)①与③和①与⑥均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为。
(8)比较⑩与⑦单质氧化性的强弱的反应的化学方程式是
比较②与⑥单质的非金属性的强弱的反应的化学方程式是