.某同学在家中发现有两瓶消毒药, 瓶外贴的信息如下:
| 化学名:高锰酸钾 别名:灰锰氧,过锰酸钾,PP粉 化学式:KMnO4 相对分子质量:158.03 性质:是一种常见的强氧化剂,常温下 为紫黑色片状晶体,见光易分解 用途:在工业上用作消毒剂、漂白剂等;医学上,用0.01%-0.02%的高锰酸钾溶液消毒、洗胃。 |
|
化学名:过氧化氢 俗名:双氧水 化学式:H2O2 相对分子质量:34 性质:无色有刺激性气味的液体,不稳定 用途:医疗上常用3%的双氧水进行伤口或中耳炎消毒。 |
依据所给信息,你认为KMnO4和H2O2的保存条件是 ;
他联系所学的化学知识,做了以下探究,请你跟他共同完成。
(1)实验室制取氧气的知识回顾
| 药 品 |
KMnO4 |
H2O2 溶液(MnO2) |
| 反应原理(写方程式) |
|
|
| 发生和收集装置(选填下图) |
|
|

(2)制取氧气的再探究
该同学想既然两种都是消毒药,能否混合使用呢?于是他进行了如下探究:
混合后观察现象:有使带火星的木条复燃的气体产生,混合液由紫红色变为无色,能使酚酞试液变红,有黑色固体产生。
①根据反应现象,该同学尝试书写了将KMnO4加入到H2O2中的化学反应方程式,
请帮他补充完整: 2 KMnO4+3 H2O2 =" 2" MnO2↓+3 O2↑+2 H2O + ;
② 该同学觉得制氧气的药品已经齐备,他又收集了家中的以下物品:
a.蜡烛,b.口服液玻璃瓶,c.吸管,d.注射器,e.小塑料瓶。
通过查阅资料得到以下信息:蜡烛火焰温度最高可达540 oC左右;高锰酸钾受热分解温度为240oC左右;口服液玻璃瓶耐高温(800oC)。
若选用KMnO4做反应物制氧气,则发生装置应选用上述物品中的 (选填字母);
若选用H2O2和MnO2制氧气,则发生装置应选用上述物品中 (选填字母);
核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题: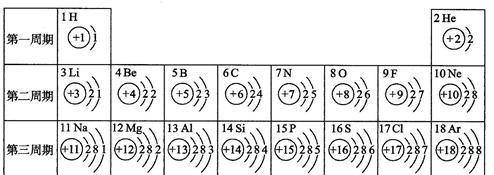
(1)在第三周期中,各原子结构的共同之处是,该周期中,各原子核外电子排布的变化规律是,
(2)在第三周期中,元素类型的变化情况是:从左到右由元素过渡到元素,并以稀有气体元素结尾。
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子,阴离子。
(4)写出含有氮元素的常见氧化物、酸、碱、盐的化学式各一个:
| 物质的类别 |
化氧物 |
酸 |
碱 |
盐 |
| 物质的化学式 |
|
|
|
以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出)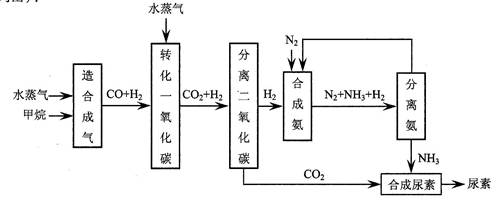
(1)尿素与熟石灰混合研磨(填"有"或"无")刺激性气味。
(2)甲烷和水蒸气在高温及催化剂的条件下反应,生成
和
,该反应的化学方程式为
(3)分离出氨后,可循环利用的两种物质是。
2013年6月5日是"世界环境日",中国主题为"同呼吸共奋斗"。
(1)化石燃料是不可再生能源,包括煤、和天然气等。
(2)下列不属于空气污染物的是。
| A. | 二氧化氮 | B. | 二氧化硫 | C. | PM2.5 | D. | 氮气 |
(3)二氧化碳是一种温室气体。某化学兴趣小组利用如下图所示装置对二氧化碳的性质进行验证: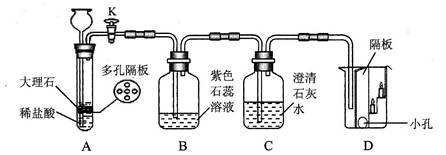
当打开K,反应一段时间后:
①D烧杯中(填"上层"或"下层")的蜡烛先熄灭,说明二氧化碳具有的物理性质是,具有的化学性质是。
②B处紫色石蕊溶液变成红色,C处澄清石灰水变浑浊。B处使紫色石蕊溶液变红的物质是;写出C处发生变化的化学方程式。
铁是应用最广泛的金属。
(1)写出铁丝在氧气中燃烧的化学方程式
(2)新型材料纳米级
粉能用作高效催化剂。实验室采用还原法制备纳米级
粉,其流程如下图所示: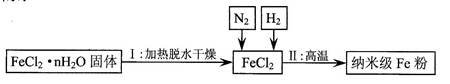
①纳米级
粉在空气中易自燃。实验中通人
的目的是。
②写出Ⅱ中
还原
,置换出铁的化学方程式。
请根据下列装置图,回答有关问题: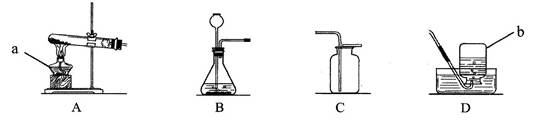
(1)写出装置图中标号仪器的名称:a,b。
(2)写出实验室用高锰酸钾制取氧气的化学方程式,
可选用的发生装置是(填字母)。
(3)写出实验室用锌粒与稀硫酸制取氢气的化学方程式,
可选用的收集装置是(填字母)。
(4)若要配制245g质量分数为10%的稀硫酸,需要质量分数为98%的浓硫酸(密度为1.84 g/cm3)ml(计算结果保留一位小数),由浓溶液配制稀溶液时,计算的依据是。在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、、混匀、冷却至室温装瓶并贴上标签。