(1)某实验小组在研究二氧化碳的性质时,根据下图进行实验。
请回答:A中的现象是______,B中反应的化学方程式是______。
(2)该小组利用对比的方法研究二氧化硫的性质,进行如下探究。
【提出问题】二氧化硫与二氧化碳均属于非金属氧化物,是否具有相似的化学性质呢?
【查阅资料】二氧化硫具有漂白性,其原因是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,实验室常用红色的品红溶液检验二氧化硫的存在。
【实验探究】实验装置如图所示。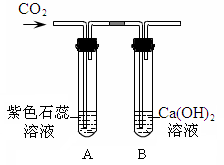
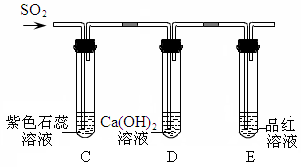
①装置C中紫色石蕊溶液变红,是由于二氧化硫与水反应生成了亚硫酸(H2SO3);装置D中澄清石灰水变浑浊,该反应的化学方程式是______。
②装置E的试管中溶液变无色,取该溶液加热,溶液又变为红色,其原因是______。
③此装置有一个明显的不足之处是______。
④活性炭也能使品红溶液褪色,其褪色原理与二氧化硫使品红溶液褪色的原理不相同,其理由是______。
【反思提高】某同学将二氧化硫通入到紫色的酸性高锰酸钾溶液中,观察到溶液由紫色变为无色,由此他得出的结论是:二氧化硫能将酸性高锰酸钾溶液漂白。请你设计实验证明此结论是否正确(要求写出操作、现象、结论):______。
二氧化硫与二氧化碳有相似的化学性质,但二氧化硫还具有某些特殊的化学性质。
下面是一些关于铁的实验研究,试按要求填空。
(1)模拟工业炼铁(装置图如右图):在硬质玻璃管内加入少量氧化铁粉末,先通入一氧化碳,排出装置内空气后,再用酒精喷灯加热A处药品。
① 硬质玻璃管内发生反应的化学方程式为: 。
② 试管B中发生反应的化学方程式为: 。
③ 该装置的主要缺点是 。
(2)铁锈蚀的探究
某化学兴趣小组进行家庭化学实验“探究铁锈蚀的原因”,设计如下图所示。他们预设的实验结果是仅有图Ⅲ中的铁钉生锈。但经过一周时间的观察,他们发现三支试管中铁钉都生锈了。
老师在听取了同学汇报后,做了如下实验帮助同学分析原因:取4份等量自来水样,经过不同的方法处理后,用数字传感器测定水样中的溶解氧,并进行如上图(Ⅰ、Ⅱ、Ⅲ)的实验。
水样溶解氧数据如下:
| 自来水 |
1号水样 |
2号水样 |
3号水样 |
4号水样 |
| 处理方法 |
不处理 |
煮沸 密封迅速冷却 |
煮沸 密封自然冷却 |
煮沸 敞口冷却 |
| 溶解氧(mg/L) |
5.37 |
0.52 |
0.66 |
3.44 |
[教师实验的现象记录(部分)]用2号水样进行的如图Ⅱ的实验中:一天后,铁钉有轻微生锈,从第二天到第七天,铁锈不再增加。
参考所给数据分析:①学生实验中:图Ⅰ中铁钉生锈的原因可能是 ;
图Ⅱ中铁钉生锈的原因可能是 。
②教师实验所记录的实验现象的原因可能是 。
如图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验.请完成实验报告:
| 实验目的 |
实验现象 |
实验结论 |
| 测定空气中 的体积分数. |
白磷着火燃烧,活塞先右移,后左移,最后 停在刻度约为 (填整数)的位置上. |
空气的成分按体积计算, 约占  . . |
某兴趣小组同学对实验室制备氧气的条件进行如下探究。
【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是 。
【设计并完成实验】
Ⅰ. 将3.0g氯酸钾放在试管中加热
Ⅱ. 将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ. 将3.0g氯酸钾与Xg氧化铜均匀混合加热
【实验现象分析】
Ⅲ中X的值应为 ,实验Ⅰ和Ⅲ比较可证明 。 现象与实验Ⅲ相同.实验Ⅱ和Ⅲ对比的目的是 。将实验Ⅲ反应后的固体加水溶解、 、洗涤、干燥,然后进行称量的目的是 ,最后还要再将黑色粉末和 混合加热,
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的化学方程式为 。
【实验反思】MnO2的用量对 H2O2分解反应有何影响?
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3%H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计。)
【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出 。图丙是“不同质量的MnO2与相同体积的3%H2O2溶液混合”的实验结果,从图中可以看出 。
用久置的镁条做实验时,需要用砂纸把表面的灰黑色打磨掉,直到露出光亮的银白色。实验小组同学对镁条表面“灰黑色外衣”的成分进行如下探究。
【提出问题】镁条表面“灰黑色外衣”的成分是什么?
【猜想与假设】
Ⅰ.是镁与空气中的氧气反应生成的氧化镁。
Ⅱ.是镁与空气中的二氧化碳反应生成的黑色碳单质。
Ⅲ.根据铜锈的成分是碱式碳酸铜,推测镁条表面的“灰黑色外衣”是镁在潮湿的空气中生锈得到的碱式碳酸镁。
同学们经讨论,从颜色上否定了只含有氧化镁,因为氧化镁是_____________。
【查阅资料】
① 碱式碳酸镁的性质有:受热可分解;常温下能与稀硫酸反应。
② 白色的硫酸铜粉末遇水能变为蓝色。
③ 碳不与稀硫酸反应,但与浓硫酸在加热条件下能反应并生成CO2、SO2和H2O。
同学们认为碳与浓硫酸反应生成三种产物的共同点是 (答出一点即可)。
【进行实验】
(1)同学们用久置的镁粉进行了如下实验。
实 验 装 置 |
 |
| 实 验 现 象 |
①无水硫酸铜粉末逐渐由白色变为蓝色 ②澄清石灰水变浑浊 |
结 论 |
久置的镁粉中除镁元素外,还含有的元素是 久置的镁粉中含有碱式碳酸镁 |
(2)同学们发现,经加热一段时间后,试管中镁粉会突然“噗”地燃烧起来,出现红热,很快停止,并有黑色固体粘附在试管壁上。
①将试管取下,冷却后加入足量稀硫酸,大部分固体溶解,并有气泡出现,但黑色固体没有消失。请写出有气体生成的一个反应化学方程式__________________。
②将实验①试管中的混合物进行_________________(填操作名称),除去其中溶液,向黑色固体中加入浓硫酸,加热。黑色固体全部溶解,得澄清溶液并伴有刺激性气味的气体产生。
实验(2)说明,镁在CO2中可以燃烧,生成了碳单质。
【实验结论】
综合上述实验现象,实验小组认为镁条表面“灰黑色外衣”中含有碳和碱式碳酸镁。
【反思与评价】
有的同学提出,实验(2)不足以证明镁条表面“灰黑色外衣”中含有碳,他的理由是_____________。
某小组同学探究二氧化碳(CO2)、氨气(NH3)分别与水反应后产物的酸碱性。他们收集了若干瓶CO2和NH3。
【确定标准】
老师指导该小组同学用自制的紫色石蕊试纸完成了如上图所示实验,确定检验酸碱性物质存在的标准。取三个洁净的表面皿,分别放上紫色石蕊试纸,向试纸上依次滴加稀盐酸、蒸馏水、氢氧化钠(碱)溶液,观察到三条试纸的颜色依次为红色、紫色和蓝色。
【实验过程】
(1)探究CO2与水反应产物的酸碱性。该小组同学向一瓶CO2中加入30 mL水,充分振荡。再取一个洁净的表面皿,放上一条紫色石蕊试纸,向试纸上滴加瓶中的液体,观察到紫色石蕊试纸变成红色,由此获得结论:瓶中液体里含有 性物质,发生反应的化学方程式为 。
(2)探究NH3与水反应产物的酸碱性。该小组同学用(1)的方法继续进行NH3的实验,他们分析液体里含有碱性物质,观察到的现象是 ,分析依据是 。
【实验反思】
有同学提出:仅用上述实验还不足以说明CO2或NH3与水发生了反应,还需补充一个对比实验,以NH3为例,该对比实验的操作为 ,观察到的现象为 。