下列各反应对应的离子方程式正确的是
| A.向Ca(OH)2溶液中加入过量的NaHCO3溶液Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
| B.向100 mL 0.12 mol/L-1的Ba(OH)2溶液中通入0.02 mol CO2:Ba2++3OH-+2CO2=HCO3-+BaCO3↓+H2O |
| C.硫酸氢钠与氢氧化钡两种溶液反应后pH恰好为7:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D.向含0.1mol/LNaOH和0.1mol/LNa2CO3的溶液中加入1L0.4mol/L稀盐酸OH-+CO32-+3H+=CO2↑+2H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.1.0mol/L的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
| C.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
| D.c(H+)/c(OH-)=1×10-13的溶液K+、Na+、CH3COO-,Br- |
下列实验能达到预项目的是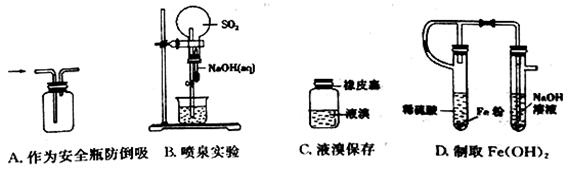
C60可用作储存氢气的材料,结构如图所示。继C60后,科学家又合成了Si60、N60,三种物质结构相似。下列有关说法正确的是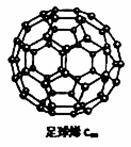
| A.C60、Si60、N60都属于原子晶体 |
| B.C60、Si60、N60分子内共用电子对数目相同 |
C.由于 键能小于 键能小于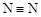 ,故N60的稳定性弱于N2 ,故N60的稳定性弱于N2 |
D.由于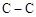 键长小于 键长小于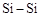 键,所以C60熔沸点低于Si60 键,所以C60熔沸点低于Si60 |
室温下,将一定浓度的一元酸HA溶液和一定浓度的NaOH溶液等体积混合(忽略体积变化),实验数据如下表:
下列判断不正确的是
A.实验①反应的溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
B.实验①反应的溶液中:c(OH-)= c(Na+)-c(A-)=Kw/(1×10-9)mol/L
C.实验②反应的溶液中:c(A-)+c(HA)>0.1mol/L
D.实验②反应的溶液中:c(Na+)= c(A-)> c(OH-)=c(H+)