原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36。已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ·mol—1 |
I1 |
I2 |
I3 |
I4 |
| X |
496 |
4562 |
6912 |
9543 |
| Y |
738 |
1451 |
7733 |
10540 |
| Z |
578 |
1817 |
2745 |
11578 |
(1)X、Y、Z的电负性从大到小的顺序为 (用元素符号表示),元素Y的第一电离能大于Z的原因是 。
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输。已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示。
①W元素基态原子价电子排布式为 。
②已知CN—与 分子互为等电子体,1molCN—中 键数目为 。
键数目为 。
③上述沉淀溶解过程的化学方程式为 。
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子价电子排布式为ns2np2,且原子半径是同族元素中最小的。
②Y元素是地壳中含量最多的元素;W在同周期中原子半径最小,在W原子的电子排布中,
p轨道上只有1个未成对电子。
③Z元素的电离能数据见下表(kJ/mol):
| I1 |
I2 |
I3 |
I4 |
…… |
| 496 |
4562 |
6912 |
9540 |
…… |
请回答:
(1)Z2Y2的电子式为___________, Z2Y2与水反应的化学方程式
(2)X、Y二种元素所形成的常见稳定的化合物的晶体类型为________ ,空间构型为________
(3)X、Y、Z、W四种元素所形成的单质中,硬度最大、熔点最高的是_____________ (填名称); XW4的结构式为_______________
(1)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液,下列说法正确的是
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+ |
| C.[Cu(NH3)4] 2+的中心离子为Cu2+ |
| D.在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3中的N原子提供空轨道 |
(2)写出(1)反应过程的离子方程式;;
在(1)得到的溶液中加入乙醇后将析出深蓝色的晶体其化学式
五种元素的原子电子层结构如下:
| A.1s22s1; | B.1s22s22p4; | C.1s22s22p6; | D.1s22s22p63s23p2 E.[Ar]3d104s1。(用元素符号作答) |
(1)元素的第一电离能最大的是 ;
(2)属于过渡元素的是 ;
(3)元素的电负性最大的是 ;
(4)上述元素之间能形成X2Y型化合物的化学式是、
已知:A、B、F是家庭中常见的有机物,F常用于食品包装,E是石油化工发展水平的标志。根据下面转化关系回答问题。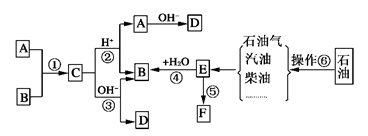
(1)分别写出A和E中官能团的名称:A中;E中;
(2) 操作⑥的名称为________________。
(3)取代反应的范畴很广,①~⑤中属于取代反应的是________(填序号)。
(4)请写出下列反应的化学方程式:
Ⅰ.C与稀硫酸溶液加热反应______________________________________;
Ⅱ.B在金属铜存在下在空气中加热反应__________________________;
Ⅲ.D的钠盐与稀盐酸反应____________________________________;
Ⅳ.F在空气中完全燃烧。
(5)F是一种常见的高分子材料,它给我们带来了巨大的方便。然而,这种材料造成的当今的某一环境问题是________________________________________。
(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准)。
| 烯类化合物 |
相对速率 |
| (CH3)2C=CHCH3 |
10.4 |
| CH3CH=CH2 |
2.03 |
| CH2=CH2 |
1.00 |
| CH2=CHBr |
0.04 |
据表中数据,总结烯类化合物加溴时,反应速率与C=C上取代基的种类、个数间的关系:。
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是(填代号)。
A.(CH3)2C=C(CH3) 2 B.CH3CH=CH CH3 C.CH2=CH2 D.CH2=CHCl