某气态烃0.5mol恰好与1molHCl加成,生成物中的氢又可被3molCl2取代,则此气态烃可能是
| A.C2H2 | B.C2H4 | C. |
D. |
向NaI和NaBr的混合溶液中通入过量的Cl2 ,充分反应后将溶液蒸干,灼热残余物,最后剩下的物质是()
| A.NaCl、I2、Cl2 | B.NaCl、I2 | C.NaCl、NaBr | D.NaCl |
在强碱性溶液中能大量共存,并且溶液为无色透明的离子组是()
A. |
B.K+、Na+、[Al(OH)4]-、NO3- |
C.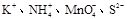 |
D.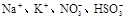 |
将过量的SO2气体通入下列溶液中,最终没有沉淀的是()
| A.Na[Al(OH) 4] | B.BaCl2 | C.Ba(NO3)2 | D.NaSiO3 |
将铁屑溶于过量的盐酸后,再加入下列物质,会有三价铁生成的是()
| A.硫酸 | B.磷酸 | C.硝酸锌 | D.氯化铜 |
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )
| A.1.2mL | B.2.4mL | C.3.6mL | D.4.8mL |