工业上制备BaCl2的工艺流程图如下: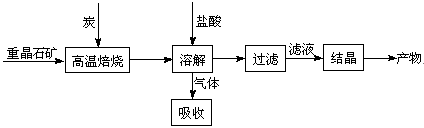
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s) 4CO(g) + BaS(s) △H1 ="+" 571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 ="+" 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) △H2=" +226.2" kJ·mol-1 ②
2CO2(g) + BaS(s) △H2=" +226.2" kJ·mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,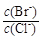 = 。
= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g) 2CO(g)的△H2= kJ·mol-1。
2CO(g)的△H2= kJ·mol-1。
⑷实际生产中必须加入过量的炭,同时还要通入空气,其目的是 , 。
(5分)现有CH4、C2H4、C2H2、C2H6、C3H8五种有机物,回答下列问题:
⑴.质量相同时,在相同状况下体积最大的是__ ____,完全燃烧时消耗O2的量最多的是__ __,生成的CO2最多的是___ _,生成水最多的是___ ___。
⑵.同温同体积时,五种物质完全燃烧耗O2的量最多的是__ ____。
(10分)分子中只含有2个碳原子的某烃A是其同系物中含碳量最高的物质; 1mol A与1mol HCl加成可得到B;1mol A与1mol H2加成可得到C,并能继续发生如下列图表所示的转变:</PGN0306.TXT/PGN>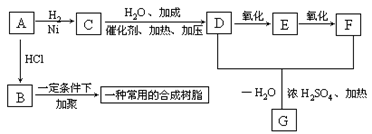
据此回答下列问题
(1) 写出实验室制取A的反应方程式 ___ _ ____________ ___ ____;
(2) 以B为原料经过加聚反应所得的合成树脂的结构简式为__ ___ _____。
(3) 写出由D和F生成G的反应方程式:
________________________ ________ __
(4) 写出E与银氨溶液反应的化学方程式:
___________ ____ ____ _________
(5) 写出符合以下两个条件的G的同分异构体,①能水解②能发生银镜反应:
医药阿斯匹林的结构简式如图1所示:
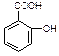
图1图2
试根据阿斯匹林的结构回答;
⑴阿斯匹林看成酯类物质,口服后,在胃肠酶的作用下,阿斯匹林发生水解反应,生成A和B 两种物质。其中A的结构简式如图2所示,则B的结构简式为;B中含有的官能团名称是。
⑵阿斯匹林跟NaHCO3同时服用,可使上述水解产物A与NaHCO3反应,生成可溶性盐随尿液排出,此可溶性盐的结构简式是。
⑶上述水解产物A与氢氧化钠溶液反应的化学方程式为
;
按要求填写:
⑴乙烯的电子式:;⑵油脂的结构通式:;
⑶甲苯制取TNT的反应方程式:;
⑷淀粉水解反应方程式:;
(8分)请选用适当的试剂和分离方法除去下列物质中所含的杂质(括号内为杂质),将所选的试剂及分离方法的编号填入表中。
试 剂: a.水 b.NaOH溶液 c.溴水 d.饱和Na2CO3溶液 e.新制CaO
分离方法:①.分液②.过滤③.洗气④.蒸馏
| 混合物 |
需加入的试剂 |
分离方法 |
| 溴苯(溴) |
||
| 乙烷(乙烯) |
||
| 乙醇(水) |
||
| 乙酸乙酯(乙酸) |