2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)用电子式表示H2O的形成过程 。
(2) H2O以 键结合(填极性键、非极性键、离子键)
(3)在pH=1的溶液中,①NH4+、Al3+、Br-、SO42- ② Na+、Fe2+、Cl-、NO3-
③K+、Ba2+、Cl-、NO3-④K+、Na+、HCO3-、SO42-四组离子中,一定大量共存的是 (填序号)。
(4)在下列反应中,水仅做氧化剂的是 (填字母,下同),水既不做氧化剂又不做还原剂的是 。
| A.Cl2+H2O=HCl+HClO | B.2Na2O2+2H2O=4NaOH+O2↑ |
| C.CaH2+2H2O=Ca(OH)2+2H2↑ | D.3Fe+4H2O Fe3O4+4H2 Fe3O4+4H2 |
(5)已知KH和H2O反应生成H2和KOH,反应中1mol KH (填失去,得到) mol电子
(6)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为 ,电极反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数约为 。
下表为元素周期表的一部分,请参照①~⑩在表中的位置,用化学用语回答下列问题:
(1)元素③形成的单质的电子式为;元素②形成的最高价氧化物的结构式为。
(2)⑥、⑦两元素的最高价氧化物的水化物之间反应的离子方程式为。
(3)②、③、④、⑤元素形成的氢化物中,热稳定性最强的是(填化学式),沸点最高的是(填化学式)。
(4)⑧、⑨元素的最高价氧化物的水化物酸性强弱比较>(填化学式)。
(5)用电子式表示⑥、⑧两元素结合成化合物的形成过程。
(6)元素⑩在周期表中的位置;该元素的单质主要用途(填一种)。
从海水中可以获得淡水、食盐并可提取镁和溴等物质。
(1)海水淡化的方法主要有(填一种)。
(2)经过化学变化才能从海水中获得的物质是(填序号)
| A.氯、溴、碘 | B.钠、镁、铝 | C.烧碱、氢气 | D.食盐、淡水 |
(3)从海水中提取镁的流程如下图所示: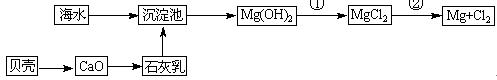
反应①的离子方程式为。
反应②的化学方程式为。
(4)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式为。
2010年4月14日7时49分在青海省玉树地区发生7.1级地震,造成了重大的人员伤亡和财产损失。为了保证震区的卫生环境,常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒,以抑制大规模传染病爆发。
回答下列问题:
(1)漂白液的有效成分是(填化学式);
(2)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质(填序号)。
| A.酸性 | B.碱性 | C.强氧化性 | D.还原性 |
(3)工业上用氯气通入石灰乳[Ca(OH)2]制取漂白粉的化学方程式:
。
(4)已知二氧化硫和亚硫酸盐具有较强的还原性。若将少量的SO2通入漂白粉溶液中,有同学认为发生的反应为:Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO。你认为该同学的说法是否正确?
(填“正确”或“不正确”),请说明理由。
(5)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一是:2NaClO3 +4HCl =2ClO2↑+ Cl2↑+ 2NaCl + 2H2O,当转移0.2mol电子时,参加反应的还原剂的物质的量为。
(6分)某种混合物中可能含有甲酸、乙酸、甲醇及甲酸乙酯这些物质中的一种或几种。在检验时有以下现象:(1)有银镜反应;(2)加入新制 悬浊液,无变澄清的现象;(3)与含碱的酚酞溶液共热,发现溶液中红色逐渐变浅以至无色。
悬浊液,无变澄清的现象;(3)与含碱的酚酞溶液共热,发现溶液中红色逐渐变浅以至无色。
根据上述现象,可以判断此混合物中一定含有,可能含有,一定没有。(填结构简式)
由中国科研人员从中药材中提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有100%的治愈率。根据下面金丝桃素的结构简式回答下列问题: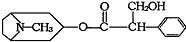
(1)金丝桃素能在NaOH水溶液中加热反应得A和B,B为芳香族化合物,写出B的结构简式:
B:,该反应属于反应。
(2)室温下,B用稀盐酸酸化得C,下列物质中不能和C发生反应的是(填序号)
①浓H2SO4和HNO3的混合液②H2(催化剂加热)
③CH3CH2CH2CH3④Na
⑤O2(催化剂加热)⑥Na2CO3溶液
(3)写出两分子C与浓H2SO4共热,生成八元环状物的化学方程式:
(4)下列物质与C互为同分异构体的有。
