已知原子序数,可能推断原子的
①质子数 ②中子数 ③质量数 ④核电荷数 ⑤核外电子数
⑥原子结构示意图 ⑦元素在周期表中的位置
| A.①②③④⑥ | B.①④⑤⑥⑦ | C.②③④⑤⑦ | D.③④⑤⑥⑦ |
能够快速、微量、精确地测定有机化合物相对分子质量的物理方法是( )
| A.质谱法 | B.红外光谱法 |
| C.紫外光谱法 | D.核磁共振氢谱法 |
下列图示的四种实验操作名称从左到右依次是( )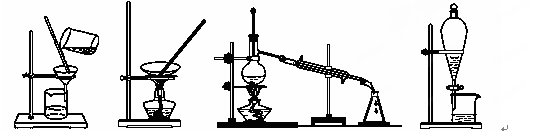
| A.蒸发、蒸馏、过滤、萃取 | B.过滤、蒸馏、蒸发、萃取 |
| C.过滤、蒸发、蒸馏、分液 | D.萃取、蒸馏、蒸发、过滤 |
常温常压下为无色液体,而且密度大于水的是( )
①苯 ②硝基苯 ③溴苯 ④四氯化碳⑤溴乙烷
⑥乙酸乙酯⑦CH3C1⑧CH3(CH2)4CH3
| A.①⑥ | B.②③④⑥ | C.②③④⑤ | D.③④⑤⑥ |
可以用分液漏斗分离的一组液体混合物是( )
| A.溴和四氯化碳 | B.苯和溴苯 | C.汽油和苯 | D.硝基苯和水 |
下列属于分离、提纯固态有机物的操作的是( )
| A.蒸馏 | B.萃取 | C.重结晶 | D.分液 |