(10分)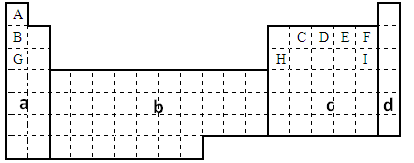
(1)在上面元素周期表中全部是金属元素的区域为___________。
| A.a | B.b | C.c | D.d |
(2)G元素单质在E元素单质中燃烧时形成的化合物的化学式是______,它是__________(填“共价化合物”或“离子化合物”)。该化合物含有的化学键类型是 ;
该化合物的电子式是 。
(3)表格中九种元素能形成最高价氧化物对应的水化物中,碱性最强的是________(用化合物的化学式表示,下同),酸性最强的是__________,属于两性氢氧化物的是__________。
(4)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是 ________(填名称),可以验证该结论的实验是_______。(填编号)
a将在空气中放置已久的这两种元素的块状单质分别放入热水中;
b将这两种元素的单质粉末分别和同浓度的盐酸反应;
c将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液;
d比较这两种元素的气态氢化物的稳定性。
(8分)写出下列物质的电离方程式
(1)Al2(SO4)3(2)CH3COOH
(3)NaHCO3(4)NaHSO4
简要回答下列问题。
(1)常温下,浓硫酸可以用铝质容器储存的原因是:
(2)墨鱼骨粉(主要成分CaCO3)可作为治疗胃酸(含盐酸)过多的药剂。其理由是:
(3)碳酸氢钠可用作焙制糕点的疏松剂的原因___________________
(4)汽车数量剧增,汽车尾气(含氮和碳的氧化物)污染日趋严重。如何控制汽车尾气污染,请你提出一条合理建议。
下表是元素周期表的一部分,针对所给的10种元素,完成下列各小题。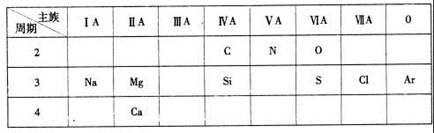
(1)第3周期中金属性最强的元素是(填元素名称);
(2)S原子结构示意图为;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是(填化学式);
(4)C、N和O原子半径由小到大的顺序的是;
(5)第3周期中气态氢化物最稳定的是;
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是,常用于制造(填一种高性能的现代通讯材料的名称);
(7)铝是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为
(8)N元素形成的一种氢化物的化学式是,俗话说“雷雨发庄稼”,请写出二氧化氮溶于水的反应为:。
(12分)(1)用50mL 0.50mol·L-1盐酸与50mL 0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题: 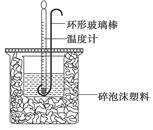
①烧杯间填满碎泡沫塑料的作用是。
②若大烧杯上改为盖薄铁板,求得的反应热数值:(填“偏大”、“偏小”或“无影响”)
③若通过测定计算产生的热量为1.42kJ,请写该反应的热化学方程式:。
(2)①已知:CH4(g)+H2O(g)===CO(g)+3H2(g)ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g)ΔH=+247.4 kJ·mol-1
则以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:。
②由气态基态原子形成1 mol化学键释放的最低能量叫键能。已知表中所列键能数据, 则
N2(g)+3H2(g) 2NH3(g) ΔH=kJ·mol-1。
2NH3(g) ΔH=kJ·mol-1。
| 化学键 |
H—H |
N—H |
N≡N |
| 键能kJ·mol-1 |
436 |
391 |
945 |
③一定条件下,在水溶液均为1 mol以下离子 Cl-、ClO-、ClO2-、ClO3-、ClO4-的能量(kJ)相对大小如下图所示,则3ClO-(aq)===ClO3-(aq)+2Cl-(aq)的ΔH=kJ·mol-1。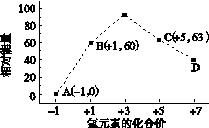
(12分,每空2分)
(1)将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经10s后达到平衡,测得SO3的浓度为0.6mol·L-1,请回答下列问题:
①用O2表示的反应的平均速率为_____________________________________
②平衡时SO2的转化率______________________________________
(2)已知某可逆反应mA(g)+nB(g)  qC(g)在密闭容器中进行。如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线。
qC(g)在密闭容器中进行。如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线。
根据图象填空
①化学计量数的关系:m+n______q;(填“>”.“<”或“=”)
②该反应的正反应为___________反应。(填“吸热”或“放热”)
(3)在FeCl3+3KSCN Fe(SCN)3+3KCl的平衡体系中,回答下列问题:(填“正向”、“逆向”、“不”)
Fe(SCN)3+3KCl的平衡体系中,回答下列问题:(填“正向”、“逆向”、“不”)
①在溶液中加入少量的KSCN固体,平衡 ______________移动。
②在溶液中加入少量的KCl固体,平衡 _____________移动。