据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是( )
| A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论 |
| B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体 |
| C.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+ |
| D.丁认为如果上述的发现存在,则证明传统的价键理论有一定的局限性有待继续发展 |
短周期主族元素A、B、C的原子序数依次递增,它们的族序数之和为11,A、C同主族,B原子最外层电子数比A原子次外层电子数多l。下列叙述不正确的是()
A.原子半径:B>C>A
B.A、C两元素的最高价氧化物对应水化物的酸性A强于C
C.C的最高价氧化物只能与碱反应,不能与任何酸反应
D.B的最高价氧化物的熔点比A的最高价氧化物的熔点低
下列化学用语的理解正确的是()
A.某离子结构示意图为: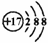 可以表示35Cl-,也可以表示37Cl- 可以表示35Cl-,也可以表示37Cl- |
B.电子式为: 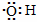 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
C.比例模型为: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 |
| D.铬元素的价电子排布式为3d44s2 |
下列叙述中,正确的是()
| A.两种元素构成的共价化合物分子中的化学键都是极性键 |
| B.含有非极性键的化合物分子一定不是极性分子 |
| C.白磷晶体中,微粒之间通过共价键结合,键角为60° |
| D.金属晶体在熔化时,金属键被破坏,而原子晶体熔化时,共价键不被破坏 |
X、Y、Z均为第三周期元素,X的第一电离能在同周期中最小,Y的电负性在同周期中最大,Z的离子半径在同周期中最小,下列关于X、Y、Z叙述中不正确的是 ()
| A.原子序数和原子半径大小顺序均为:X<Y<Z |
| B.元素X与元素Y能形成离子化合物 |
| C.元素Z最高价氧化物对应水化物具有两性 |
| D.元素Y形成的气态氢化物水溶液呈强酸性 |
已知次氯酸分子的结构式为H—O—Cl,下列有关说法正确的是()
| A.依据其结构判断该含氧酸为强酸 | B.O原子与H、Cl都形成σ键 |
| C.该分子为极性分子 | D.该分子的电子式是H︰O︰Cl |