请你参与某学习小组研究性学习的过程,并协助完成相关任务。
【研究课题】探究水壶内部水垢的主要成分
【查阅资料】通过查阅资料知道,天然水和水垢所含的物质及其溶解性如下表:
| 物 质 |
Ca(HCO3)2 |
Mg(HCO3)2 |
Ca(OH)2 |
Mg(OH)2 |
CaCO3 |
MgCO3 |
| 溶解性 |
可溶 |
可溶 |
微溶 |
不溶 |
不溶 |
微溶 |
【提出猜想】水垢的主要成分一定含有Mg(OH)2和 ,可能含有Ca(OH)2和 。
【设计方案】
(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,静置。取上层清液滴入Na2CO3溶液,如果没有白色沉淀,说明水垢中无 (填化学式)。
(2)乙同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分。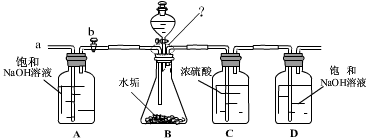
其主要实验步骤如下:
①按图组装仪器,将50g水垢试样放入锥形瓶中,逐滴加入足量稀盐酸。若D瓶增重22g,则水垢全部是CaCO3。
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气;
③称量D瓶内物质增加的质量;
④重复②和③的操作,直至D瓶内物质质量不变。
测量滴加稀盐酸体积与D瓶内物质增加质量的关系如图曲线所示;
【评价】
①A瓶中的NaOH溶液起到 作用。若A瓶中无NaOH溶液,D瓶中的质量将 (填“增大”、“不变”或“减小”)。
②一般情况下,两种不同金属形成的碳酸盐与足量盐酸反应时,若两金属的化合价相同、两种盐的质量相同,则相对分子质量小者放出的气体多。分析曲线图可知:水垢中一定含有(化学式),理由是 。
③装置图中“?”所指处有三根导管同时穿过橡胶塞,已知:导管的直径为8mm,橡胶塞细段直径为3cm。从坚固和美观的角度考虑,请你在由图中标出应在哪三点打孔为好(用圆圈“○”表示打孔位置)。
以上实验 (填“能够”或“不能”)检测出水垢中含有Mg(OH)2。
我们已经学过实验室制取气体的一般思路和方法,请利用下列装置回答相关问题.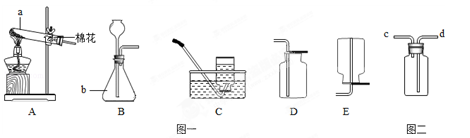
(1)写出图一中a和b的仪器名称:ab;
(2)选择图一中的装置制取和收集二氧化碳气体,那么应选择的装置是和;
在实验室中制取二氧化碳气体的常用药品:液体是,固体是。
(3)若要用图二装置收集二氧化碳气体,则气体应从(填c或d)端通.理由是.
(4)用制取的二氧化碳进行如下有关性质实验:
①实验(II)中溶液变色;
②实验(III)中加热之后,溶液又变为色,解释出现此现象的原因。
(5)实验室用高锰酸钾制取氧气的化学反应方程式(或化学式表达式)若要用排水法收集一瓶较纯净的氧气,开始收集氧气的最佳时机是。
(6)同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,乙同学发现用排水法收集到的O2大于理论产量。针对这一现象,同学们进行了如下探究:
[提出猜想]猜想I:反应生成的MnO2分解放出O2;
猜想II:反应生成的K2MnO4分解放出O2;
猜想III:反应生成的K2MnO4和MnO2分解都放出O2。
[实验验证]同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。该组同学选择的实验方法是。
[拓展延伸]实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快。
请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么?。
有一次晚自修时,学校突然停电,同学们点起了蜡烛,不一会儿来电了,大家把蜡烛吹灭,这时看到有一缕白烟,有几个同学对这缕白烟产生了兴趣。
【提出问题】小明想,吹灭蜡烛时观察到的一缕白烟的成分是什么?
【猜想与假设】小亮猜测白烟是蜡烛燃烧产生的二氧化碳;小光猜想白烟是石蜡燃烧产生的水蒸气;小明猜想白烟是石蜡蒸气凝结成的固体颗粒。
【收集证据】
(1)查阅资料:烟是由固体颗粒形成的,雾是由小液滴形成的。石蜡的熔点和沸点都很低,很容易液化和气化。二氧化碳是无色的且能使澄清石灰水变浑浊的气体。
(2)实验探究:①吹灭蜡烛,立即用一个内壁涂有澄清石灰水的烧杯罩住白烟,观察到澄清石灰水。小亮得出结论:白烟是二氧化碳。但小明对此提出质疑,小明认为小亮不正确的原因是。
②吹灭蜡烛,立即用一块干而冷的玻璃片罩在白烟上,玻璃片上没有水雾。小光得出结论:白烟不是。
③吹灭蜡烛,立即用燃着的木条靠近白烟,发现蜡烛重新被点燃,说明白烟具有可燃性,该实验同时排除了的猜想。
【得出结论】以上探究结果可知:的猜想是正确的。
某校化学兴趣小组的同学利用下列装置进行实验。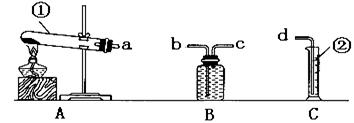
实验目的:
一.用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验。
二.粗略测定加热2g高锰酸钾所收集到的氧气体积。
反应原理:(用化学式表达式表示)
高锰酸钾制氧气:。
细铁丝在氧气中燃烧: 。
装置连接:
写出标数字的仪器名称:①,②。
为达到实验二的目的,各装置的正确连接顺序是:(填接口的字母)a→→ →d。
问题分析:
(1)实验过程发现B瓶中的水变红了,原因是:。
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作可能是:。
(3)在本实验中,收集氧气的时机是加热后马上收集,若是在气体连续不断产生之后才开始收集,则测得的氧气的体积会比实际值(填“偏大”或“偏小”或“不变”)。
(4)实验结束时,乙同学发现收集到的氧气大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】
猜想I:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的二氧化锰装入试管,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变.则猜想错误。
②第二组同学取锰酸钾装入试管,在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是。
某化学研究性学习小组在做“寻找新的催化剂”课题时,发现将生锈的铁钉放到过氧化氢溶液中,也可以加快过氧化氢的分解速率。于是,他们对此展开探究:
【提出问题】什么物质是该反应催化剂?
【猜想与假设】:下面是组内两位同学所作的猜想,请你完成小华的猜想。
小芳同学:铁钉表面的铁锈(氧化铁)是过氧化氢溶液分解反应的催化剂。
小华同学:铁钉里的是过氧化氢溶液分解反应的催化剂。
【实验与结论】
| 实验操作 |
实验现象 |
实验结论 |
| 实验I:把一定质量的氧化铁粉末加入到装有10mL5%的过氧化氢溶液的试管中,并用一根带火星的小木条置于试管口,观察现象。 |
反应的文字表达式为: 假设一成立 |
|
| 实验Ⅱ:取10mL5%的过氧化氢溶液于另一支试管中,加入,并用一根带火星的小木条置于试管口,观察现象。 |
无现象 |
假设二 (填“成立”或“不成立”) |
【讨论交流】同学们讨论后认为,小芳的“实验I”还不能够确切的说明氧化铁就是过氧化氢分解制取氧气的催化剂,理由是:。
请你设计实验(写出实验步骤、实验现象及结论)证明其中的某一点理由:
(如果可以,你将获得4分的奖励分,但卷面总分不得超过60分)
| 实验操作 |
实验现象 |
实验结论 |
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间。
【进行实验】如图是他们进行实验的装置图,气体发生装置中A仪器名称是,此实验中B处宜采用的气体收集方法是。 
【实验记录】
| 实验编号 |
1 |
2 |
| 反应物 |
6% H2O2溶液 |
6% H2O2溶液 |
| 催化剂 |
1g红砖粉 |
1g MnO2 |
| 时间 |
152秒 |
35秒 |
 【结论】该探究过程得出的结论是。
【结论】该探究过程得出的结论是。
【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明
MnO2和红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的和是否改变。
H2O2生成O2的快慢还与哪些因素有关?请你帮助他们继续探究。(只要求提出假设和实验方案)
【假设】。
【实验方案】。