CO和H2在一定条件下可以合成乙醇:2CO(g) + 4H2(g) 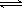 CH3CH2OH(g)+ H2O(g)
CH3CH2OH(g)+ H2O(g)
下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
| A.CO全部转化为乙醇 |
| B.正反应和逆反应的化学反应速率均为零 |
| C.CO和H2以1:2的物质的量之比反应生成乙醇 |
| D.反应体系中乙醇的物质的量浓度不再变化 |
下列反应的离子方程式书写正确的是:
| A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN-= Fe(SCN)3↓ |
| B.向海带灰浸出液中加入稀硫酸、双氧水:2I- + 2H+ + H2O2= I2 + 2H2O |
| C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-= Na2SiO3↓+H2O |
| D.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+ OH-+ Ba2+ = H2O + BaCO3↓ |
下列说法正确的是
| A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 |
| C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,,即布朗运动 |
| D.电解MgCl2饱和溶液,可制得金属镁 |
1 L某混合溶液中,溶质X、Y的浓度都为0.1 mol/L,向混合溶液中滴加某溶液Z(0.1 mol/L的氢氧化钠或硫酸溶液),所得沉淀的物质的量随着Z溶液的体积变化关系如图所示,则X、Y、Z分别是
| A.AlCl3、 FeCl3、 NaOH | B.AlCl3、 MgCl2、 NaOH |
| C.NaAlO2、Ba(OH)2、H2SO4 | D.NaAlO2、BaCl2、 H2SO4 |
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是 ( )
| X |
Y |
Z |
|
| ① |
NaOH溶液 |
Al(OH)3 |
稀硫酸 |
| ② |
KOH溶液 |
SiO2 |
浓盐酸 |
| ③ |
O2 |
N2 |
H2 |
| ④ |
FeCl3溶液 |
Cu |
浓硝酸 |
A. ①③ B.①④ C.②④ D.②③
卫生部发出公告,自2012年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。下列对于过氧化钙(CaO2)的叙述错误的是 ( )
| A.CaO2具有氧化性,对面粉可能具有增白作用 |
| B.CaO2中阴阳离子的个数比为1∶1 |
| C.CaO2与水反应时,每产生1 mol O2转移电子4 mol |
| D.CaO2与CO2反应的化学方程式为2CaO2+2CO2===2CaCO3+O2 |