元素的性质随着元素原子序数的递增而呈周期性变化的原因是
| A.元素原子的核外电子排布呈周期性变化 |
| B.元素的原子半径呈周期性变化 |
| C.元素的化合价呈周期性变化 |
| D.元素的金属性、非金属性呈周期性变化 |
下列说法正确的是
| A.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s)的ΔH<0 |
| B.常温下,BaSO4分别在相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中的溶解度相同 |
| C.常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) |
| D.等体积、等物质的量浓度的NH3·H2O溶液与NH4Cl溶液混合后溶液呈碱性,说明NH3·H2O的电离程度小于NH4+的水解程度 |
一种三室微生物燃料电池污水净化系统原理如右图所示,图中有机废水中有机物可用C6H10O5表示。下列有关说法正确的是
| A.b电极为该电池的负极 |
| B.b电极附近溶液的pH减小 |
| C.a电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+ |
| D.中间室:Na+移向左室,Cl-移向右室 |
X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
| A.X与Y形成的化合物只有一种 |
| B.R的氢化物的热稳定性比W的强 |
| C.原子半径:r(Z)<r(R) |
| D.Y的最高价氧化物的水化物的酸性比W的强 |
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
| 物质 组别 |
甲 |
乙 |
丙 |
| A |
SO2 |
Ba(OH)2 |
NaHCO3 |
| B |
Na2O2 |
H2O |
CO2 |
| C |
Na2SiO3 |
NaOH |
HCl |
| D |
Al |
H2SO4 |
NaOH |
下列指定反应的离子方程式正确的是
| A.Cu与浓硝酸反应制备NO2:3Cu+8H++2NO3-===3Cu2++2NO2↑+4H2O |
| B.NH4Al(SO4)2溶液与过量NaOH溶液反应:Al3++4OH-===AlO2-+2H2O |
C.用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-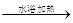 CH3COO-+NH4++3NH3+2Ag↓+H2O CH3COO-+NH4++3NH3+2Ag↓+H2O |
| D.用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2===I2+2OH- |