2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的,回收利用锂资源成为重要课题。某研究小组对某废旧锂离子电池正极材料(图中简称废料,成份为LiMn2O4、石墨粉和铝箔)进行回收研究,工艺流程如下: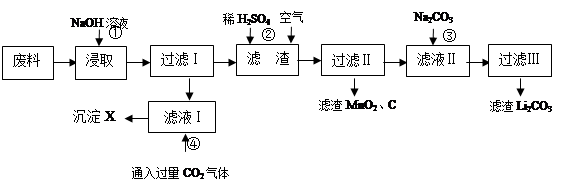
已知:Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g。
(1)废料在用NaOH溶液浸取之前需要进行粉碎操作,其目的是 。
(2)废旧电池可能由于放电不完全而残留有锂单质,为了安全对拆解环境的要求______ __ 。
(3)写出反应④生成沉淀X的离子方程式:
。
(4)己知LiMn2O4中Mn的化合价为+3和+4价,写出反应②的离子反应方程式:
。
(5)生成Li2CO3的化学反应方程式为______ __。已知Li2CO3在水中的溶解度随着温度升高而减小,最后一步过滤时应_ _。
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
1) 写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):
写出产物即可不需要配平
2)整个过程中的还原剂是。
3)把KI换成KBr,则CCl4层变为色:继续滴加氯水,CCl4层的颜色没有变化。由此推测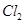 、
、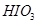 、
、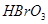 氧化性由强到弱的顺序是。
氧化性由强到弱的顺序是。
(1)在S+2KNO3+3C=K2S+N2+3CO2的反应中元素被氧化,元素被还原;
是氧化剂,是还原剂;是氧化产物,是还原产物。
(2)某物质A在一定条件下加热分解,产物都是气体,分解方程式为:
2A(s)=" B(g)" + 2C(g) + 2D(g),取一定量的A加热,完全分解,同温同压下测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为。
(3)现有A、B、C、D四瓶溶液,它们分别是NaCl(0.1mol?L-1)、HCl(0.1mol?L-1)、NaOH(0.1mol?L-1)和酚酞试液(0.1%)中的一种。有人不用其他试剂,就可以把它们一一鉴别开来,其实验步骤如下:
①各取溶液少许两两混合,据现象不同分成两组;
②取一组混合液,不断滴入另一组的一种未知溶液,根据现象不同可鉴别出A和B两种溶液;
③再取已鉴别出A溶液2mL, 滴入3滴未知C溶液,再加入D溶液4mL,在这个过程中无明显颜色变化;
综合以上实验可知,A、B、C、D溶液分别是:
A; B; C; D。
常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。
(1)铁粉与水蒸气反应的化学方程式是:
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法:
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(结合化学方程式说明):
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是:
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如下图所示的装置:
请简述实验操作及原理:
威斯迈尔反应是在富电子芳环上引入甲酰基的有效方法。其过程首先是N,N-二甲基甲酰胺与POCl3反应生成威斯迈尔试剂:
接着威斯迈尔试剂与富电子芳环反应,经水解后在芳环上引入甲酰基。例如: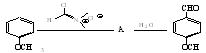
10-1用共振式表示威斯迈尔试剂正离子。
10-2由甲氧基苯转化为对甲氧基苯甲醛的过程中,需经历以下步骤:⑴芳香亲电取代⑵分子内亲核取代⑶亲核加成⑷质子转移⑸消除。画出所有中间体的结构简式。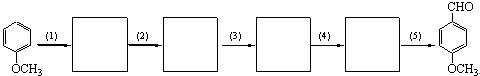
10-3完成下列反应: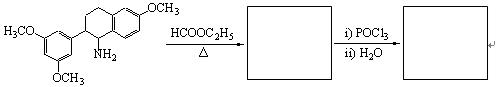
化合物A、B和C的分子式均为C7H8O2。它们分别在催化剂作用和一定反应条件下加足量的氢,均生成化合物D(C7H12O2)。D在NaOH溶液中加热反应后在酸化生成E(C6H10O2)和F(CH4O)。
A能发生如下转化: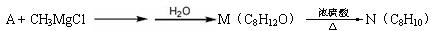
生成物N分子中只有3种不同化学环境的氢,它们的数目比为1∶1∶3。
9-1 画出化合物A、B、C、D、E、M和N的结构简式。
9-2 A、B和C互为哪种异构体?(在正确选项的标号前打钩)
①碳架异构体②位置异构体③官能团异构体④顺反异构体
9-3 A能自发转化为B和C,为什么?
9-4 B和C在室温下反应可得到一组旋光异构体L,每个旋光异构体中有个不对称碳原子。