将二氧化硫通入溴水中发生如下的反应:SO2+Br2+2H2O=2HBr+H2SO4,反应中转移的电子数和还原剂是
| A.2e-,H2SO4 | B.4e-,SO2 | C.2e-,Br2 | D.2e-,SO2 |
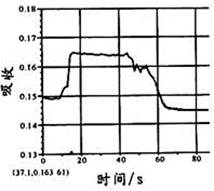
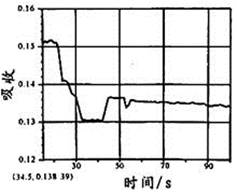
在图1所示密闭容器中充满红棕色的NO2气体,当迅速将活塞向右推一段距离后保持活塞不动时,色度计测出颜色变化的情况如图2所示。如果迅速将活塞往左拉一段距离后保持活塞不动时,色度计测出颜色变化的情况正确的图示为

A. B.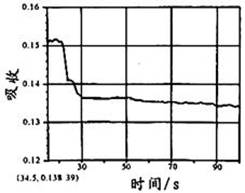

C. D .
苹果iphone5正在我国热卖,其电池为锂电池。构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6 LiCoO2+6C,下列说法错误的是
LiCoO2+6C,下列说法错误的是
| A.该电池的负极为LiCoO2 |
| B.电池中的固体电解质可以是氯化钠、干冰等 |
| C.充电时的阴极反应:Li1-xCoO2+xLi++xe-=LiCoO2 |
| D.外电路上的“→”表示放电时的电子流向 |
碘与氢气反应的热化学方程式为:
①I2(g)+H2(g) 2HI(g) ΔH=" -" 9.48 kJ·mol-1
2HI(g) ΔH=" -" 9.48 kJ·mol-1
②I2(s)+H2(g) 2HI(g) ΔH=" +" 26.48 kJ·mol-1,由此判断下列说法或反应正确的是
2HI(g) ΔH=" +" 26.48 kJ·mol-1,由此判断下列说法或反应正确的是
| A.反应①的产物比反应②的产物稳定 |
B.I2(s) I2(g)ΔH=" +" 17.00 kJ·mol-1 I2(g)ΔH=" +" 17.00 kJ·mol-1 |
| C.反应②的反应物总能量比反应①的反应物总能量低 |
| D.1 mol I2(g)中通入1 mol H2(g),反应后放热9.48 kJ |
反应 PCl5(g)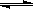 PCl 3(g)+Cl2(g)①
PCl 3(g)+Cl2(g)①
2HI(g)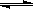 H2(g)+I2(g)②
H2(g)+I2(g)②
2NO2(g)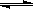 N2O4(g)③
N2O4(g)③
在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则转化率
| A.均不变 | B.均增大 |
| C.①增大,②不变,③减少 | D.①减少,②不变,③增大 |
可逆反应A(g)+B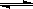 C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到达平衡时,下列叙述不正确的是
C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到达平衡时,下列叙述不正确的是
| A.若保持恒容,充入C气体后混合气体颜色加深,则说明B是有颜色的气体 |
| B.若升高温度,发现C的物质的量减少,则说明正反应为放热反应 |
| C.若压缩容器,平衡不移动,则说明B和D一定都是气体 |
| D.保持恒容,到达平衡后继续充入A会使B的转化率增大,A的转化率减少 |