(10分)在常温常压下,都用惰性材料作电极.分别电解(同浓度、同体积、通过相同电量)下列溶液:
| A.CuSO4 | B.AgNO3 | C.KOH | D.H2SO4 E.NaCl F.Na2SO4 |
通电一段时间切断电源,请填写下列空白。
(1)在A中一个电极上质量增加了0.128 g,在B中一个电极上质量增加 ,增加的物质是 .
(2) 在一极产生O2,同时另一极产生H2(填写序号,下同).
(3) 电解后,溶液中的C(OH-)增大
(4) 电解后,溶液的pH减小.
(5) 电解后,溶液的浓度增大而[H+]不变.
磺酰氯(SO2Cl2)是一种有机氯化剂,也是锂电池正极活性物质。已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解。
(1)已知:SO2 (g) +Cl2 (g)+ SCl2 (g) 2SOCl2 (g) △H="a" kJ·mol-1
2SOCl2 (g) △H="a" kJ·mol-1
SO2Cl2(g)+ SCl2 (g)  2SOCl2(g) △H="b" kJ·mol-1
2SOCl2(g) △H="b" kJ·mol-1
则反应:SO2(g) + Cl2 (g) SO2Cl2(g) △H =kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K =。
SO2Cl2(g) △H =kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K =。
(2)磺酰氯可与白磷发生反应为:P4+ 10SO2Cl2= 4PCl5 + 10SO2↑,若生成1molSO2,则转移电子的物质的量为mol。
(3)某学习小组的同学依据反应:SO2(g)+ Cl2(g) SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图。
SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图。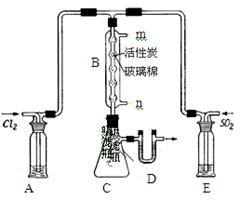


①若用浓盐酸与二氧化锰为原料制取Cl2,其反应的化学方程式为。
②上图所示的装置说法正确的是(不定项选择)。
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和Na2SO3溶液
b.B处反应管内五球中玻璃棉上的活性炭作催化剂
c.B处反应管冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
③从化学平衡移动角度分析,反应管通水冷却的目的为。
(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如图所示,
已知电池反应为:2Li + SO2Cl2 =" 2LiCl" + SO2↑;则电池工作时,正极的电极反应式为。
(14分)高铁酸盐在能源、环保等方面有着广泛的用途。高铁酸钾(K2FeO4)易溶于水,具有强氧化性,是一种新型水处理剂。替代传统的净水剂及Cl2对淡水进行净化消毒是城市饮用水处理新技术。
工业上常用如下方法制备高铁酸钾:以铁丝网为阳极电解NaOH溶液,然后在阳极液中加入50%的KOH溶液,充分反应后,过滤、用异丙醇洗涤、干燥,即可制得。
(1)高铁酸钾具有强氧化性的原因是。
(2)用异丙醇代替水洗涤产品的好处是。
(3)高铁酸钾是一种理想的水处理剂,其处理水的原理为,。
(4)高铁电池是正在研制中的可充电干电池,下图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有、。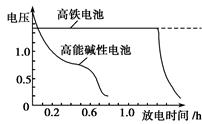
(5)探究高铁酸钾的某种性质。
[实验1]将适量K2FeO4固体分别溶解于pH为4.74、7.00、11.50的水溶液中,配得FeO42-浓度为1.0 mmol·L-1(1 mmol·L-1=10-3 mol·L-1)的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。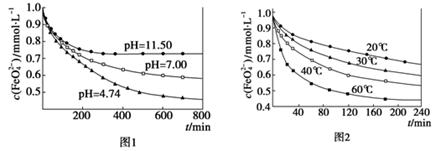
[实验2]将适量K2FeO4溶解于pH=4.74的水溶液中,配制成FeO42-浓度为1.0 mmol·L-1的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则
①实验1的目的是;
②实验2可得出的结论是;
③高铁酸钾在水中的反应为4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2↑。
4Fe(OH)3+8OH-+3O2↑。
由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是。
某合作学习小组的同学拟用硼砂制取硼酸并测定硼酸样品的纯度。制备硼酸的实验流程如下:
(1)溶解硼砂时需要的玻璃仪器有:烧杯和。
(2)用pH试纸测定溶液pH的操作方法为。
(3)用盐酸酸化硼砂溶液生成硼酸的离子方程式为。
(4)实验流程中缺少的步骤a、步骤b操作分别为、。
(5)硼酸酸性太弱不能用碱的标准溶液直接滴定,实验室常采用间接滴定法,其原理为: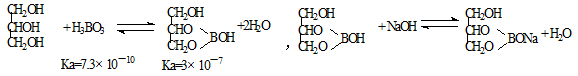
滴定步骤为:
①滴定到终点时溶液颜色变化是。
②若滴定到终点时消耗NaOH标准溶液22.00mL,则本次滴定测得的硼酸样品中硼酸的质量分数为(假定杂质不反应)。
③若滴定时滴定管尖嘴部分有气泡,滴定过程中消失,将导致测得的结果(选填:“偏大”、“偏小”或“不变”)。
钾水玻璃以其优异的性能广泛用于防腐、铸造、油田、钻井或各种高档涂料中。钾水玻璃中硅含量的测定可以采用氟硅酸钾容量法,其步骤为:
①称取试样溶解在含有过量的氟离子和钾离子的强酸溶液中,硅能与氟离子、钾离子作用生成氟硅酸钾(K2SiF6)沉淀;
②沉淀分离后于热水中水解,生成HF、H2SiO3、KF;
③过滤除去硅酸沉淀,用氢氧化钠标准溶液滴定滤液。
(1)上述步骤②中的水解反应方程式为;
步骤③中反应的离子方程式为:。
(2)在步骤③中,若滴定前未用氢氧化钠标准溶液润洗滴定管,则测得的硅元素含量将(填“偏高”、或“偏低”或“不变”)。
(3)若每次称取试样的质量为1.00g,重复滴定四次,消耗1.00 mol·L-1氢氧化钠标准溶液的体积为分别为16.80mL、19.90mL、20.00mL、20.10mL,试计算该试样中硅元素的质量分数(以二氧化硅计),写出计算过程。
(12分)海水中含有丰富的镁资源。工业上常用海水晒盐后的苦卤水提取Mg,流程如下图所示:
(1)工业制取镁的方法是法。
(2)试剂Ⅰ一般选用(填化学式)。
(3)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。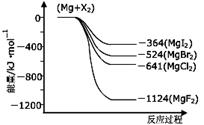
①由图可知Mg与卤素单质的反应均为(填“放热”或“吸热”)反应;推测化合物的热稳定性顺序为MgI2MgF2(填“>”、“=”或“<”)。
②依上图数据写出MgBr2(s)与Cl2(g)反应的热化学方程式。
(4)金属Mg与CH3Cl在一定条件下反应可生成CH3MgCl,CH3MgCl是一种重要的有机合成试剂,易与水发生水解反应并有无色无味气体生成。写出CH3MgCl水解的化学方程式。